题目内容
金属在生成生活中应用广泛.
(1)下列制品中,主要利用金属导电性的是 (填序号).
A.铁锅 B.铜导线 C.铝箔
(2)春季停止供暖后,暖气管道最好注满水以防止生锈,其原理是 ;
(3)废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为 ;
(4)兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液.他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:
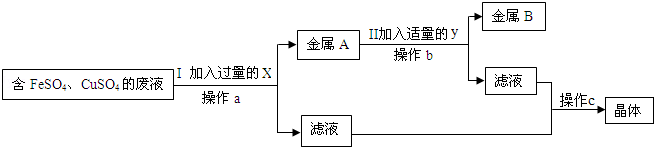
①操作C的名称为 ;
②写出Ⅰ中有关反应的化学方程式 ;
③Ⅱ加入适量的y时发现有气泡产生,说明金属A中的物质为 .此步反应的方程式为 .
(1)下列制品中,主要利用金属导电性的是 (填序号).
A.铁锅 B.铜导线 C.铝箔
(2)春季停止供暖后,暖气管道最好注满水以防止生锈,其原理是 ;
(3)废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为 ;
(4)兴趣小组的同学从实验室中收集一桶含有FeSO4、CuSO4的废液.他们想从中回收金属铜和硫酸亚铁晶体,设计了如下方案:

①操作C的名称为 ;
②写出Ⅰ中有关反应的化学方程式 ;
③Ⅱ加入适量的y时发现有气泡产生,说明金属A中的物质为 .此步反应的方程式为 .
故答案为:(1)B;(2)隔绝氧气;(3)3CO+Fe2O3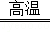 2Fe+3CO2 ;(4)①蒸发;②Fe+CuSO4=Cu+FeSO4;③铁和铜;Fe+H2SO4=H2↑+FeSO4.
2Fe+3CO2 ;(4)①蒸发;②Fe+CuSO4=Cu+FeSO4;③铁和铜;Fe+H2SO4=H2↑+FeSO4.
 2Fe+3CO2 ;(4)①蒸发;②Fe+CuSO4=Cu+FeSO4;③铁和铜;Fe+H2SO4=H2↑+FeSO4.
2Fe+3CO2 ;(4)①蒸发;②Fe+CuSO4=Cu+FeSO4;③铁和铜;Fe+H2SO4=H2↑+FeSO4.试题分析:(1)A.铁锅是主要利用铁的导热性;B.铜导线主要利用铜的导电性;C.铝箔主要利用铝的延展性;(2)铁生锈是铁与氧气和水接触,暖气管道最好注满水是隔绝了氧气;(3)反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,根据得失氧进行配平,反应条件是高温,所以方程式是:3CO+Fe2O3
 2Fe+3CO2 (4)①从硫酸亚铁溶液中析出硫酸亚铁是利用蒸发溶剂,将水除去即可;②由题意可知,由于需要将铜离子转化为铜单质,而溶液还必须为硫酸亚铁,即不能引入新的杂质,所以可以加入铁将铜离子转化为铜单质,反应物是铁和硫酸铜写在等号的左边,生成物是铜和硫酸亚铁,写在等号的右边,所以方程式是:Fe+CuSO4=Cu+FeSO4;③为了将硫酸铜中的铜全部置换出来,需要加入过量的铁,所以金属A中有铜和过量的铁;由于铜与硫酸不反应,铁和硫酸反应,所以加入硫酸将铜与铁分开,加入过量稀硫酸的目的是除去铜中的铁,反应物是铁和硫酸写在等号的左边,生成物是硫酸亚铁和氢气,写在等号的右边,所以反应的方程式是:Fe+H2SO4=H2↑+FeSO4.
2Fe+3CO2 (4)①从硫酸亚铁溶液中析出硫酸亚铁是利用蒸发溶剂,将水除去即可;②由题意可知,由于需要将铜离子转化为铜单质,而溶液还必须为硫酸亚铁,即不能引入新的杂质,所以可以加入铁将铜离子转化为铜单质,反应物是铁和硫酸铜写在等号的左边,生成物是铜和硫酸亚铁,写在等号的右边,所以方程式是:Fe+CuSO4=Cu+FeSO4;③为了将硫酸铜中的铜全部置换出来,需要加入过量的铁,所以金属A中有铜和过量的铁;由于铜与硫酸不反应,铁和硫酸反应,所以加入硫酸将铜与铁分开,加入过量稀硫酸的目的是除去铜中的铁,反应物是铁和硫酸写在等号的左边,生成物是硫酸亚铁和氢气,写在等号的右边,所以反应的方程式是:Fe+H2SO4=H2↑+FeSO4.
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目