题目内容
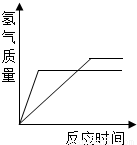
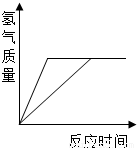
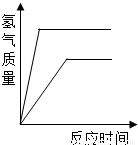
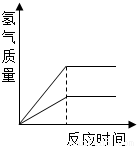
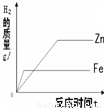
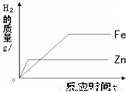
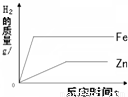
相同质量的Zn、Fe分别与足量稀盐酸作用,产生H2的质量与反应时间关系如下图所示,其中正确的是( )
分析:相等质量的锌和铁分别与足量的稀盐酸反应,由于稀盐酸过量,因此充分反应后放出氢气的质量大小由金属决定;根据金属活动性强弱关系锌>铁,可判断锌与稀盐酸反应快,铁与稀盐酸反应慢,即金属与锌的反应时间最短最先完成、铁完成的反应消耗时间长.
解答:解:由于稀盐酸过量,因此充分反应后放出氢气的质量大小由金属决定,根据化学方程式Fe+2HCl=FeCl2+H2↑知每56g铁生成2g氢气,根据化学方程式Zn+2HCl=ZnCl2+H2↑知每65g锌反应生成2g氢气,所以相等质量的铁和锌与足量稀盐酸反应铁生成氢气多,对于图象铁的终点纵坐标应该大于锌,可排除选项AB;根据金属活动性强弱关系锌>铁,可判断锌与稀盐酸反应快,铁与稀盐酸反应慢,即金属与锌的反应时间最短最先完成、铁完成的反应消耗时间长.对于图象又可排除选项D.
故选C.
故选C.
点评:变化曲线类问题,需要关注曲线的起点、折点及趋势,根据这三个方面的特殊意义,可正确分析曲线与变化的关系.

练习册系列答案
相关题目