题目内容
【题目】2012年伦敦奥运会主场馆“伦敦碗”(见图)所用的钢材量只有2008年北京主场馆“鸟巢”钢材量的1/3,堪称物美价廉,将为奥运史留下一笔宝贵的遗产。

(1)钢铁是使用最多的金属材料。生铁和钢都是铁合金,其中含碳量较高的是____。大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度____(填“大”或“小”)。
(2)英国是老牌工业强国。工业上常以焦炭、赤铁矿(主要成分是氧化铁Fe2O3)、空气等为主要原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式____________;
(3)伦敦碗场馆中被混凝土严密包裹的钢筋不易生锈的原因是________。请你举出其他的防止金属制品生锈的措施有________
【答案】生铁 大 Fe2O3+3CO![]() 2Fe+3CO2 隔绝空气(或氧气)和水 涂防锈漆、使用不锈钢等
2Fe+3CO2 隔绝空气(或氧气)和水 涂防锈漆、使用不锈钢等
【解析】
(1)钢铁是使用最多的金属材料。生铁和钢都是铁合金,其中含碳量较高的是生铁(含碳量2%![]() 4.3%)。大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度大。
4.3%)。大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度大。
(2)英国是老牌工业强国。工业上常以焦炭、赤铁矿(主要成分是氧化铁Fe2O3)、空气等为主要原料炼铁,一氧化碳与氧化铁在高温下反应产生铁和二氧化碳的化学方程式:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(3)伦敦碗场馆中被混凝土严密包裹的钢筋不易生锈的原因是:钢筋与潮湿的空气隔绝。防止金属制品生锈的措施有:涂防锈漆、使用不锈钢等;

 第1卷单元月考期中期末系列答案
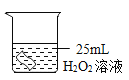
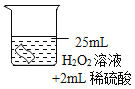
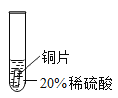
第1卷单元月考期中期末系列答案【题目】过氧化氢(H2O2)在生产生活中有着广泛的应用,化学实验小组对过氧化氢溶液的腐蚀性进行研究,将铜片分别浸泡在以下3种溶液中进行实验,实验现象如下表,有关叙述不正确的是
编号 | ① | ② | ③ |
实验 |
|
|
|
一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小汽包 | 无明显变化 |
A.实验①的作用是对照作用
B.实验②中溶液变蓝,因为反应中生成了CuSO4
C.实验③中无明显变化,说明铜不能与稀硫酸反应
D.实验②中产生细小气泡,是因为发生置换反应产生了氢气
【题目】铬(Cr)是一种重要的金属材料,具有良好的金属光泽和抗腐蚀性,常用来镀在其他金属的表面上,铜、铬锰、镍组成合金可以制成各种性能的不锈钢。实验中学化学小组同学以“比较铬、铝、铜三种金属的活动性”为课题进行探究。
(查阅资料)(1)铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
(2)铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液。
(提出猜想)小组考虑到铝的活动性比铜强,对3种金属的活动性顺序作出如下猜想.猜想一:铬>铝>铜;猜想二:铝>铜>铬;猜想三:铝>铬>铜
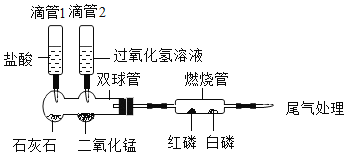
(实验过程)相同温度下,取大小相同、表面打磨光亮的铬、铝、铜三种金属薄片,分别投入等体积等溶质质量分数的足量稀硫酸中(反应中Cr显+2价),
实验一 | 实验二 | 实验三 | |
实验 方案 |
|
|
|
实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色。 | _____ | 铝片表面产生气泡较快。 |
结论 | 铬能和稀硫酸发生反应,反应速率较慢。 | 铜不与稀硫酸反应 | ____ |
三种金属在金属活动性顺序中猜想_____正确。 | |||
(分析拓展)(1)不锈钢是一种____(填“纯净物“”或“混合物”),三种金属片用砂纸打磨光亮的目的是____。
(2)实验一所发生反应的化学方程式是____。
(3)第一小组提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是_____。
(4)第二小组认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是______。
(共同归纳)比较金属活动性强弱的方法有①____,②_____。