题目内容
【题目】实验室制取氢气的化学方程式_____________。其发生装置与制取__________气体相同。收集方法有_________,因为___________。或者是_________,因为___________。氢气的化学性质是(1)可燃性,反应方程式____________________;(2)还原性,氢气还原氧化铜的反应方程式_____________________________。
【答案】 Zn+H2SO4=ZnSO4+H2↑ 二氧化碳 向下排空气法 其密度小于空气的密度 排水法 其难溶于水 2H2+O2![]() 2H2O H2+CuO
2H2O H2+CuO![]() Cu+ H2O
Cu+ H2O
【解析】氢气具有可燃性和还原性;氢气难溶于水,密度比空气小。实验室制取氢气的化学方程式是Zn+H2SO4=ZnSO4+H2↑。其发生装置与制取二氧化碳气体相同,均属于固体和液体反应不需加热制取气体。收集方法有向下排空气法,因为其密度小于空气的密度。或者是排水法,因为其难溶于水。氢气的化学性质是(1)可燃性,反应方程式是2H2+O2![]() 2H2O;(2)还原性,氢气还原氧化铜的反应方程式是H2+CuO
2H2O;(2)还原性,氢气还原氧化铜的反应方程式是H2+CuO![]() Cu+ H2O。
Cu+ H2O。
点睛∶氢气具有可燃性和还原性。氢气难溶于水,可以用排水法收集;密度比空气小,也可以用向下排空气法收集。

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案【题目】下表列出了固体物质A在不同温度时的溶解度:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 36 | 35 | 34 | 33 | 32 | 31 | 30 | 29 | 28 | 27 |
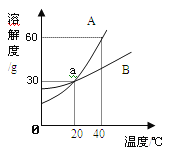
(1)70℃时,向盛有100g水的烧杯中加入30g固体A,充分溶解形成的是______________(填“饱和”或“不饱和”)溶液,再将烧杯内物质温度降至20℃,此时溶液中溶质与溶剂的质量比为_____________(填最简整数比);
(2)通过对上表数据的分析,物质A的溶解度曲线应是右图中的___________(填“甲”或“乙”);
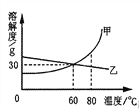
(3)80℃时,配制一定量A物质的溶液,将其降温到60℃,是否有固体析出?____________(填“有”、 “没有”或“不确定”)。
【题目】M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是____________ 。
【设计与实验一】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸);
实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 |
刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 |
几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 |
【交流与表达】同学们对同一实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中无气泡产生的原因,该原因是_____________。
【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:

(1)试管乙中观察到的现象是_________________________ 。
(2)试管丙中反应的化学方程式为_______________________ 。
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管____________(填试管编号)中的实验,也可以得出正确的结论。
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序。
【评价与反思】实验结束后,同学们对实验过程进行了如下反思:
(1)影响金属与酸反应速率快慢的因素,除了相互反应的金属和酸的性质外,还有_____________(任写一种)