题目内容
【题目】实验室中有一瓶部分变质了的NaOH溶液,小丽为了测定溶液中溶质的Na2CO3的质量分数,现取20g待测溶液,向其中逐滴加入CaCl2溶液,产生沉淀质量与所加CaCl2质量的关系如图所示.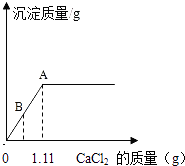
(1)B点处所得溶液中溶质有 .
(2)若加入的CaCl2溶液的质量分数为11.1%,则需该溶液的质量为
(3)求待测溶液中Na2CO3的质量分数.( 写出计算过程)
【答案】
(1)Na2CO3、NaOH和NaCl
(2)10g
(3)解:设溶液中Na2CO3的质量为x
Na2CO3+ | CaCl2═CaCO3↓+2NaCl |
106 | 111 |
x | 1.11g |
![]() 解得:x=1.06g
解得:x=1.06g
待测溶液中Na2CO3的质量分数为: ![]() =5.3%
=5.3%
答:待测溶液中Na2CO3的质量分数为5.3%.
【解析】(1)由于Na2CO3+CaCl2═CaCO3↓+2NaCl,由图可以看出,B点处溶液中的碳酸钠没有完全反应,溶液中的溶质有:Na2CO3、NaOH和NaCl;
(2)CaCl2溶液的质量为: ![]() =10g;
=10g;
(3)设溶液中Na2CO3的质量为x
Na2CO3+ | CaCl2═CaCO3↓+2NaCl |
106 | 111 |
x | 1.11g |
![]() 解得:x=1.06g
解得:x=1.06g
待测溶液中Na2CO3的质量分数为: ![]() =5.3%
=5.3%
答:待测溶液中Na2CO3的质量分数为5.3%.
所以答案是:(1)NaCl、Na2CO3、NaOH;(2)10g;(3)5.3%
【考点精析】通过灵活运用根据化学反应方程式的计算,掌握各物质间质量比=系数×相对分子质量之比即可以解答此题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目