题目内容
某同学对一种无色溶液进行鉴定实验,试根据他实验报告中的步骤和现象,填写相应的实验结论.(该溶液只含一种溶质)
2.选用石灰石、氧气、盐酸和铁为原料各写一个符合要求的化学反应方程式.
(1)化合反应 .
(2)分解反应 .
(3)置换反应 .
(4)复分解反应 .
| 实验步骤 | 实验现象 | 结论 |
| a取该溶液少许,向其中加几滴酚酞试液 | 溶液无变化 | 该溶液一定不显 |
| b另取该溶液少许,向其中加入锌粒,并用燃着的细木条放在试管口; | 有无色气体放出,该气体能燃烧,火焰呈淡蓝色; | 生成的气体是 |
| c再取该溶液少许,向其中加硝酸银溶液,再加入足量的稀硝酸. | 有白色沉淀生成,该沉淀不溶于稀硝酸. | 白色沉淀为 |
(1)化合反应
(2)分解反应
(3)置换反应
(4)复分解反应
考点:证明盐酸和可溶性盐酸盐,书写化学方程式、文字表达式、电离方程式
专题:物质的鉴定题,化学用语和质量守恒定律
分析:由题意可知:向无色溶液中加入酚酞试液后,酚酞试液不变色,该溶液一定不显碱性;
向无色溶液中加入锌粒,有无色气体放出,该气体能燃烧火焰呈淡蓝色,可知,该气体为氢气,同时也说明该溶液的溶质属于酸类;
向溶液中向其中加硝酸银溶液,再加入足量的稀硝酸.,产生白色沉淀,白色沉淀不溶于稀硝酸,说明该酸的溶液中含有氯离子,该沉淀为氯化银,该溶液为盐酸.
2.首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
向无色溶液中加入锌粒,有无色气体放出,该气体能燃烧火焰呈淡蓝色,可知,该气体为氢气,同时也说明该溶液的溶质属于酸类;
向溶液中向其中加硝酸银溶液,再加入足量的稀硝酸.,产生白色沉淀,白色沉淀不溶于稀硝酸,说明该酸的溶液中含有氯离子,该沉淀为氯化银,该溶液为盐酸.
2.首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答:解:由实验报告中的步骤和现象可知:
无色溶液不能使酚酞试液变色,该溶液一定不显碱性;
该溶液与锌反应生成气体能燃烧,产生淡蓝色火焰,可推出:气体为氢气,该溶液为酸的溶液;
向该溶液中向其中加硝酸银溶液,再加入足量的稀硝酸,产生了白色沉淀,说明了该沉淀不溶于稀硝酸,应为氯化银,溶液中含有氯离子.
综合以上分析,该溶液为盐酸.
故答为:碱; 氢气;酸;氯化银;盐酸.
2.:(1)铝片与氧气反应生成氧化铝,属于化合反应,反应的化学方程式为:3Fe+2O2═Fe3O4;
(2)石灰石的主要成分是碳酸钙,高温下生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3
CaO+CO2↑.
(3)铝与稀盐酸反应生成氯化铝和氢气,属于置换反应,反应的化学方程式为:Fe+2HCl=FeCl2+H2↑;
(4)石灰石与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故答案为:(1)3Fe+2O2
Fe3O4;(2)CaCO3
CaO+CO2↑;(3)Fe+2HCl=FeCl2+H2↑;(4)CaCO3+2HCl═CaCl2+H2O+CO2↑.
无色溶液不能使酚酞试液变色,该溶液一定不显碱性;
该溶液与锌反应生成气体能燃烧,产生淡蓝色火焰,可推出:气体为氢气,该溶液为酸的溶液;
向该溶液中向其中加硝酸银溶液,再加入足量的稀硝酸,产生了白色沉淀,说明了该沉淀不溶于稀硝酸,应为氯化银,溶液中含有氯离子.
综合以上分析,该溶液为盐酸.
故答为:碱; 氢气;酸;氯化银;盐酸.
2.:(1)铝片与氧气反应生成氧化铝,属于化合反应,反应的化学方程式为:3Fe+2O2═Fe3O4;
(2)石灰石的主要成分是碳酸钙,高温下生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3
| ||
(3)铝与稀盐酸反应生成氯化铝和氢气,属于置换反应,反应的化学方程式为:Fe+2HCl=FeCl2+H2↑;
(4)石灰石与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故答案为:(1)3Fe+2O2
| ||
| ||
点评:本题主要考查盐酸的鉴定方法,特别在鉴定时,加硝酸银溶液,再加入足量的稀硝酸,要排除CO32-等其它离子的干扰.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
如图是元素周期表中的一格,从该图获取的信息是( )
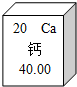

| A、该元素的质子数为40 |
| B、该元素的原子序数为20 |
| C、该元素在地壳中的含量为40.00% |
| D、该元素属于非金属元素 |
 如图是a、b、c三种物质的溶解度曲线,请据图回答:
如图是a、b、c三种物质的溶解度曲线,请据图回答: