题目内容
【题目】小华在实验室用氯酸钾和二氧化锰制氧气,加热一段时间后停止实验(氯酸钾未完全分解),他测得剩余物质中两种金属元素的质量分数分别为:锰元素质量分数11.0%,钾元素的质量分数39.0%,请问剩余物质中氧元素的质量分数为( )
A.6.4%
B.14.5%
C.25.5%
D.50%
【答案】B
【解析】解:用氯酸钾和二氧化锰制氧气,加热一段时间后停止实验(氯酸钾未完全分解),则剩余物质为氯酸钾和二氧化锰、氯化钾,而钾元素和氯元素的质量比为39:35.5,则剩余物质中氯元素的质量分数为39.0%× ![]() =35.5%;则剩余物质中氧元素的质量分数为1﹣11.0%﹣39.0%﹣35.5%=14.5%.
=35.5%;则剩余物质中氧元素的质量分数为1﹣11.0%﹣39.0%﹣35.5%=14.5%.
故选B.
实验室用氯酸钾和二氧化锰制取氧气,其中二氧化锰为反应的催化剂,在反应前后质量不变,因为化学变化中元素质量不变,加热氯酸钾制取氧气的过程中,氯元素质量不变,而钾元素和氯元素的质量比不变,由锰元素质量分数11.0%,钾元素的质量分数39.0%,可以计算出剩余物质中氧元素的质量分数.

【题目】按照体积计算空气中氧气约占21%,某化学兴趣小组的同学按照课本的实验装置做“测定空气中氧气的体积分数”实验(图1),但测出的氧气体积分数明显偏小.请你参与探究:
(1)【提出问题】造成误差的原因是什么?如何改进课本实验装置?
【查阅资料】①
颜色、状态 | 熔点/℃ | 燃烧所需最低温度/℃ | 密度/gcm﹣3 | |
红磷 | 暗红色固体 | 590 | 240 | 2.34 |
白磷 | 白色固体 | 44.1 | 40 | 1.82 |
②二氧化碳气体能被氢氧化钠溶液吸收
③在加热的条件下铜粉能与氧气反应生成黑色的氧化铜固体
【猜想】
甲同学:可能是导管内原存有空气,后来留有吸入的水,影响实验的准确性;
乙同学:可能是瓶内残留气体中还有氧气的缘故;
你还能做的猜想是(写一点即可).
(2)【交流与讨论】
①写出图1中集气瓶中发生反应的符号表达式;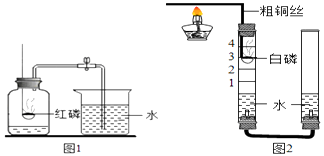
②丙同学认为,用木炭代替红磷也能完成图1的实验,但事先要在集气瓶中放入一定量的;
(3)他们对图1实验装置进行了如图2的改进.
①甲同学提出应把红磷更换为白磷,理由是;
②通过粗铜丝来点燃玻璃管内的白磷,利用了金属铜的性;
(4)【探究与反思】
①为验证乙同学的猜想,将铜粉在残余气体中加热,观察到铜粉变黑,所以乙同学的猜想(选填“合理”或“不合理”);
②大家采用改进的实验装置(图2)进行实验(左边玻璃管上面的空气平均分成了5等份,并标刻度线),待玻璃管冷却、管内白色的烟幕消失,同时能观察到 .
(5)图2的玻璃管中预先装一定量的水,是为了:①加快气体的冷却;② .