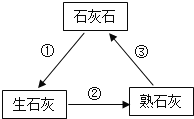
题目内容
某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品6 g,放入20 g水中使其完全溶解,再加入稀盐酸26.2 g,恰好完全反应,反应后溶液的总质量为50 g。
试计算:(写出计算过程,结果保留一位小数)
(1)生成二氧化碳的质量;
(2)样品中Na2CO3的质量分数;
(3)反应后所得溶液中溶质的质量分数。
练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
化学课上,老师在一瓶充满CO2软塑料瓶中加入适量NaOH溶液,振荡,发现软塑料瓶变瘪。针对这一有趣的现象,同学们发表自己的见解,请参与其中,并完成下列问题。
(1)小亮同学该现象说明了CO2和NaOH确实发生了反应。塑料瓶变瘪的原因是_____,二者反应的化学方程式为_____。小芳同学提出了质疑,她认为上述实验不足以证明CO2和NaOH确实发生了反应,其原因是_____。
(2)要证明一个反应是否发生,可以从以下两个角度思考。
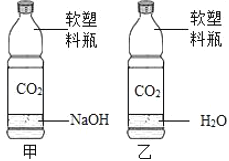
①证实反应物减少。我思考后,设计了如图所示的甲、乙对照实验,该实验需要控制的变量有_____,实验现象是_____。
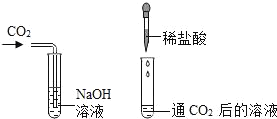
②证实有新物质生成。小霞同学为证明有碳酸钠生成,设计如下实验方案,我们帮她完成。
实验步骤和方法 | 实验现象 | 实验结论 | |
方案一 |
| _____ | CO2和NaOH确实发生了反应 |
方案二 | _____ | _____ |
写出方案二中所涉及的反应化学方程式_____。
(3)由此探究,我得到的启示是_____。(写出一点即可)