题目内容
小明同学在滴加FeCl3溶液时,不小心把滴加FeCl3溶液的滴管放入到盛“双氧水”(过氧化氢)的试剂瓶中,发现有大量的气泡产生.小明联想到用二氧化锰可做为过氧化氢分解的催化剂,他想FeCl3溶液中含有H2O、Fe3+、和Cl-这三种微粒哪一种能真正催化分解H2O2呢?于是他做了以下的几个猜想(请你一起参与并填写下列的空白):猜想1:真正催化分解H2O2的不是FeCl3溶液中的H2O,因为H2O2的溶液中已经有H2O.
猜想2:真正催化分解H2O2的是FeCl3溶液中的Fe3+
猜想3:______
他对猜想2和猜想3,进行了实验探究,请你帮忙他填写下表:
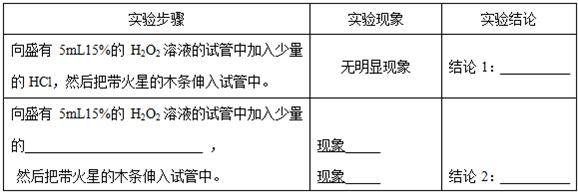
| 实验步骤 | 实验现象 | 实验结论 |
| 向盛有5mL15%的H2O2溶液的试管中加入少量的HCl,然后把带火星的木条伸入试管中. | 无明显现象 | 结论1:_______________ |
| 向盛有5mL15%的H2O2溶液的试管中加入少量的______________,然后把带火星的木条伸入试管中. | 现象________ 现象________ | 结论2:_______________ |
【答案】分析:FeCl3溶液对过氧化氢分解有催化作用,其中含有H2O、Fe3+、和Cl-三种粒子,可以排除H2O的催化作用,对于Fe3+和Cl-是否有催化作用要分别通过实验验证,验证的方法是分别取含有这两种离子的试剂进行实验,然后根据现象判断.
解答:解:因为FeCl3溶液中含有H2O、Fe3+、和Cl-三种粒子,H2O、Fe3+ 属于猜想1和猜想2,那么猜想3就是:真正催化分解H2O2的是FeCl3溶液中的Cl-.验证Cl-可用盐酸,结果没有现象,可以得出结论:真正催化分解H2O2的不是FeCl3溶液中的Cl-
验证Fe3+可用硝酸铁溶液,根据现象,可以得出结论:真正催化分解H2O2的是FeCl3溶液中的Fe3+
故答案:真正催化分解H2O2的是FeCl3溶液中的Fe3+
点评:验证一种溶液具有催化作用,要把溶液中所含的粒子逐一分析,根据现象得出结论.
解答:解:因为FeCl3溶液中含有H2O、Fe3+、和Cl-三种粒子,H2O、Fe3+ 属于猜想1和猜想2,那么猜想3就是:真正催化分解H2O2的是FeCl3溶液中的Cl-.验证Cl-可用盐酸,结果没有现象,可以得出结论:真正催化分解H2O2的不是FeCl3溶液中的Cl-
验证Fe3+可用硝酸铁溶液,根据现象,可以得出结论:真正催化分解H2O2的是FeCl3溶液中的Fe3+
故答案:真正催化分解H2O2的是FeCl3溶液中的Fe3+
| 实验步骤 | 实验现象 | 实验结论 |
| 结论1:真正催化分解H2O2的不是FeCl3溶液中的Cl- | ||
| 硝酸铁溶液 | 现象1:有许多气泡产生 现象2:木条复燃 | 结论2:真正催化分解H2O2的是FeCl3溶液中的Fe3+ |
点评:验证一种溶液具有催化作用,要把溶液中所含的粒子逐一分析,根据现象得出结论.

练习册系列答案
相关题目
一次化学实验课上,小明同学在滴加FeCl3溶液时,不小心把盛有FeCl3溶液的滴管误放入盛“双氧水”(过氧化氢溶液)的试剂瓶中了,但他发现有大量的气泡产生.小明联想到二氧化锰可以做过氧化氢分解的催化剂,那么FeCl3溶液是否也可以做过氧化氢分解的催化剂呢?于是他和同学们对此问题进行了实验与探究.
(1)[提出问题]FeCl3溶液能否做过氧化氢分解的催化剂
(2)[猜想与假设]FeCl3溶液可以做过氧化氢分解的催化剂
(3)[设计与实验]请你帮助他们填写下表:
| 实验步骤 | 实验现象 | 实验结论 |
| ①在试管中加入5mL15%的“双氧水” ②滴入适量的FeCl3溶液 ③把带火星木条伸入试管 | FeCl3溶液可以催化分解过氧化氢 |
①能够催化分解过氧化氢的粒子是FeCl3溶液中的H2O
②能够催化分解过氧化氢的粒了是FeCl3溶液中的Fe3+
③能够催化分解过氧化氢的粒子是FeCl3溶液中的Cl-
你认为最不可能的是哪一种猜想?其理由是______.
小明和同学们又对余下的两种猜想,进行了实验探究,请你帮助他们填写下表:
| 实验步骤 | 实验现象 | 实验结论 |
| ①向盛有5mL15%的“双氧水”的试管中加入少量盐酸,然后把带火星木条伸入试管 | 无明显现象 | ______ |
| ②向盛有5mL15%的“双氧水”的试管中加入少量______溶液,然后把带火星木条伸入试管 | ______ | ______ |