题目内容
【题目】如图为实验室常用的实验装置,请回答问题: 
(1)写出带有标号仪器的名称:①;② .
(2)若用A、C装置组合制取氧气,实验中,观察到水槽中气泡(填“刚一冒出”或“连续均匀冒出”)时,开始收集.收集完毕时,应先(填“熄灭酒精灯”或“从水中取出导气管”).
(3)写出用B、E装置组合制取某气体的化学反应方程式 .
(4)硫化氢是有毒气体,能溶于水形成氢硫酸(其化学性质与盐酸相似).常用块状硫化亚铁(FeS)和稀硫酸在常温发生复分解反应制H2S,某同学用G装置来收集处理H2S. ①实验室制H2S的化学方程式为;
②该装置用于收集H2S,说明其密度比空气(填“大”或“小”);
③用化学方程式表示氢氧化钠溶液的作用是 , 漏斗的作用是 .
【答案】
(1)分液漏斗;集气瓶
(2)连续均匀冒出;从水中取出导气管
(3)H2SO4+Zn=ZnSO4+H2↑
(4)H2SO4+FeS=FeSO4+H2S↑;大;2NaOH+H2S=Na2S+2H2O;防止溶液倒吸(入集气瓶)
【解析】解:(1)①是分液漏斗,②是集气瓶;(2)用排水法收集的时机不能是刚一冒气泡,否则收集到的是空气使氧气不纯;收集完毕若先熄灭酒精灯会引起水的倒流使试管炸裂,故应该先从水中取出导气管;(3)BE组合适合制取固液常温型的反应及密度比空气小的气体,因此可以是熟悉的氢气用活泼金属和酸反应制得,故方程式为:H2SO4+Zn=ZnSO4+H2↑或其他合理答案;(4)①硫化亚铁(FeS)和稀硫酸发生复分解反应,因此产物为:硫酸亚铁和硫化氢,反应的方程式为:H2SO4+FeS=FeSO4+H2S↑;②根据收集方法及进气管(长管)可以判断硫化氢的密度比空气大;③因为硫化氢有毒,能溶于水形成氢硫酸,故可以和氢氧化钠发生酸碱中和反应,从而防止多余的硫化氢逸散到空气中污染空气;漏斗可以增大与氢氧化钠的接触面积,防止溶液倒吸入集气瓶. 所以答案是:(1)①分液漏斗 ②集气瓶(2)连续均匀冒出 从水中取出导气管(3)H2SO4+Zn=ZnSO4+H2↑或其他合理答案(4)①H2SO4+FeS=FeSO4+H2S↑ ②大 ③2NaOH+H2S=Na2S+2H2O 防止溶液倒吸(入集气瓶)
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号.

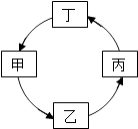
【题目】下表所列各组物质中,物质之间较下图箭头方向,通过一步反应就能实现转化的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
A | Cu | CuO | CuSO4 | Cu(OH)2 |
B | Na2CO3 | CaCO3 | CaO | Ca(OH)2 |
C | H2SO4 | Na2SO4 | BaSO4 | Ba(OH)2 |
D | CO2 | CaCO3 | H2O | O2 |
A.A
B.B
C.C
D.D
【题目】亮亮做家务时接触到下列用品.
用品 | 洁厕灵 | 炉灶清洁剂 |
有效成分 | 盐酸 | 氢氧化钠 |
(1)洁厕灵有效成分是盐酸,盐酸是一种重要的化工产品,也是实验室中重要的化学试剂,增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是 , 打开一瓶浓盐酸可以看到瓶口出现 .
(2)据图分析下列符号各代表哪种粒子: 
![]()
![]()
![]() .
.
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是 .
(4)做完家务,他用Vc泡腾片冲了一杯饮料,Vc泡腾片主要成分为维生素C(C6H8O6),柠檬酸(C6H8O7)、碳酸氢钠、不属于有机物的是 .