题目内容
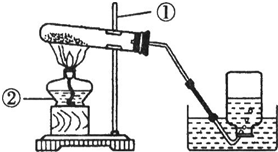
某同学用氯酸钾制取干燥、较纯净的氧气.实验步骤如下:①、检查装置气密性,气密性良好; ②、先在试管中放入MnO2,再放入略多于计算量的KClO3; ③、连接好实验装置 ④、加热 ⑤、收集气体 ⑥、适当的时间后,停止加热,撤卸装置.
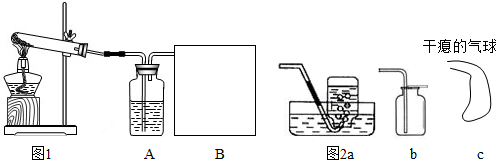
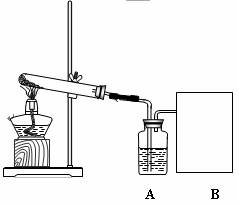
(提示:装置A中所装试剂是浓硫酸,它作干燥剂,可吸收水蒸气.)回答下列问题:
(1)该实验的化学符号表达式为
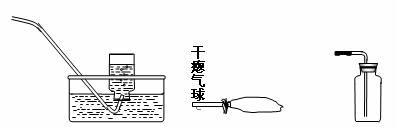
(2)方框中最好选用下列装置中的
(3)实验中观察到何种现象时开始收集气体?
(4)实验结束后,该同学发现收集到的氧气比预计的少很多,百思不得其解.你认为可能的原因是
分析:(1)根据反应物与生成物及反应条件来书写化学方程式;
(2)根据制取干燥、较纯净的氧气来选择收集气体的装置;
(3)装置中开始有空气,需要等空气被氧气排干净时才能收集气体;
(4)当收集到的氧气比预计的少很多时,利用反应原理来分析解答.
(2)根据制取干燥、较纯净的氧气来选择收集气体的装置;
(3)装置中开始有空气,需要等空气被氧气排干净时才能收集气体;
(4)当收集到的氧气比预计的少很多时,利用反应原理来分析解答.
解答:解:(1)因反应物为氯酸钾,生成物为氧气,根据元素守恒还应生成氯化钾,在二氧化锰作催化剂并加热下发生化学反应,故答案为:2KClO3
2KCl+3O2↑;
(2)因a用排水法,不能得到干燥的氧气,b用向上排空气法会导致气体不纯,c为直接收集,故答案为:c.
(3)因开始产生的氧气能将装置中的空气排出,只有当气泡均匀连续冒出时才是纯净的氧气,此时可以收集,故答案为:A瓶管口气泡均匀、连续冒出时.
(4)由氯酸钾分解的方程式可以看出,若反应不完全,则氧气的量就少,故答案为:KClO3未完全分解.
| ||
| △ |
(2)因a用排水法,不能得到干燥的氧气,b用向上排空气法会导致气体不纯,c为直接收集,故答案为:c.
(3)因开始产生的氧气能将装置中的空气排出,只有当气泡均匀连续冒出时才是纯净的氧气,此时可以收集,故答案为:A瓶管口气泡均匀、连续冒出时.
(4)由氯酸钾分解的方程式可以看出,若反应不完全,则氧气的量就少,故答案为:KClO3未完全分解.
点评:本题考查了利用加热法分解制氧气的有关问题,应紧扣实验的要求和实验装置图来分析,并应明确每部分装置的作用来解答.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
 :
:

 实验室常用于制取氧气的方法有:a、加热氯酸钾固体;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气.
实验室常用于制取氧气的方法有:a、加热氯酸钾固体;b、加热高锰酸钾固体;c、用二氧化锰粉末作催化剂使过氧化氢(H2O2)溶液分解产生水和氧气.