题目内容
写出下列变化的化学方程式,并按要求填写所属反应类型:(1)实验室用过氧化氢制氧气 属于 反应.
(2)“曾青(CuSO4)得铁化为铜” 属于 反应.
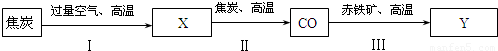
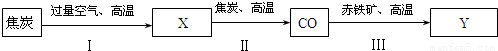
(3)高炉炼铁中,一氧化碳与氧化铁在高温下反应 .
(4)酸雨形成中的亚硫酸(H2SO3)与氧气作用生成硫酸 .
(5)我国发射神舟飞船所用的长征捆绑式火箭,是用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作为液体燃料.偏二甲肼在四氧化二氮中充分燃烧,生成一种空气中含量最多的气体和两种氧化物并放出能量. .
【答案】分析:根据题目中的叙述分析出反应物、生成物、反应条件,然后根据书写方程式的原则进行方程式的书写,依据反应中的反应物和生成物的特点以及各种反应类型的基本特征确定反应的类型.
解答:解:(1)反应物是双氧水,生成物是水和二氧化碳,反应条件是二氧化锰作催化剂,该反应是一种物质反应生成了两种物质,故答案为:2H2O2 2H2O+O2↑,分解;
2H2O+O2↑,分解;
(2)反应物是铁和硫酸铜,生成物是硫酸亚铁和铜,反应不需条件,该反应是单质和化合物反应生成了单质和化合物,故答案为:Fe+CuSO4═FeSO4+Cu,置换;
(3)反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,反应条件是高温,所以方程式为:3CO+Fe2O3 3CO2+2Fe;
3CO2+2Fe;
(4)反应物是亚硫酸和氧气,生成物是硫酸,所以方程式为:2H2SO3+O2═2H2SO4;
(5)反应物偏二甲肼(C2H8N2)和四氧化二氮(N2O4),生成物是二氧化碳、氮气和水,反应条件是点燃,所以方程式为:C2H8N2+2N2O4 3N2↑+2CO2↑+4H2O.
3N2↑+2CO2↑+4H2O.
点评:根据给出的反应物、生成物书写化学方程式以及判断反应类型是近几年中考的热点,要进行识记.
解答:解:(1)反应物是双氧水,生成物是水和二氧化碳,反应条件是二氧化锰作催化剂,该反应是一种物质反应生成了两种物质,故答案为:2H2O2
 2H2O+O2↑,分解;
2H2O+O2↑,分解;(2)反应物是铁和硫酸铜,生成物是硫酸亚铁和铜,反应不需条件,该反应是单质和化合物反应生成了单质和化合物,故答案为:Fe+CuSO4═FeSO4+Cu,置换;
(3)反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,反应条件是高温,所以方程式为:3CO+Fe2O3
 3CO2+2Fe;
3CO2+2Fe;(4)反应物是亚硫酸和氧气,生成物是硫酸,所以方程式为:2H2SO3+O2═2H2SO4;
(5)反应物偏二甲肼(C2H8N2)和四氧化二氮(N2O4),生成物是二氧化碳、氮气和水,反应条件是点燃,所以方程式为:C2H8N2+2N2O4
 3N2↑+2CO2↑+4H2O.
3N2↑+2CO2↑+4H2O.点评:根据给出的反应物、生成物书写化学方程式以及判断反应类型是近几年中考的热点,要进行识记.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目