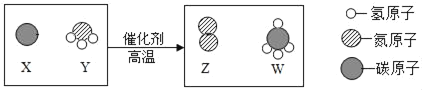
��Ŀ����
����Ŀ����֪a��b��c��d��eΪ��1��3���ڵ�Ԫ�أ���ԭ��������������bΪϡ������Ԫ�أ�c��d��Ԫ�ؿ���������ֳ���������ڳ��³�ѹ�£���Ϊ��ɫ��ζ�����壬����һ��������Ѫ�쵰�Ľ��������ǿ����һ��������ʹ�ó����ʯ��ˮ����ǣ�dΪ�ؿ��ﺬ������Ԫ�أ�eΪ�ؿ��ﺬ�����Ľ���Ԫ�ء�
��1��a��Ԫ�ط���Ϊ��_____��
��2��b���ʻ�ѧ���ʱȽϣ�_____��ѡ��ȶ������á�����
��3��cԪ������������Ļ��ϼ۷ֱ�Ϊ��_____��_____��
��4��dԪ�ص�ԭ�ӽṹʾ��ͼΪ��_____��
��5���ڿ����е�ȼa���ʵĻ�ѧ����ʽΪ��_____��
��6��e���ʺ�ϡ������Һ��Ӧ�Ļ�ѧ����ʽΪ��_____��
���𰸡�H �ȶ� +2 +4  2H2 + O2
2H2 + O2![]() 2H2O 2Al + 6HCl = 2AlCl3 + 3H2��
2H2O 2Al + 6HCl = 2AlCl3 + 3H2��
��������
c��d��Ԫ�ؿ���������ֳ���������ڳ��³�ѹ�£���Ϊ��ɫ��ζ�����壬����һ��������Ѫ�쵰�Ľ��������ǿ����һ��������ʹ�ó����ʯ��ˮ����ǣ�һ����̼��Ѫ�쵰�Ľ��������ǿ��������̼��ʹ�ó����ʯ��ˮ����ǣ�c��d��Ԫ����̼Ԫ�غ���Ԫ���е�һ�֣�c��dԭ������������������c��̼��d����Ԫ�أ�eΪ�ؿ��ﺬ�����Ľ���Ԫ�أ�e����Ԫ�أ�bΪϡ������Ԫ�أ�a��b��c��d��eΪ��1-3���ڵ�Ԫ�أ���ԭ��������������b�Ǻ�Ԫ�أ���a����Ԫ�ء�����ԭ�⣬����������
�������Ϸ�����֪��
��1��a����Ԫ�أ�Ԫ�ط���Ϊ��H��
��2��b��̼Ԫ�أ��䵥����̼����ѧ���ʱȽ��ȶ���
��3��cԪ������������ֱ�ΪCO��CO2����Ԫ�صĻ��ϼ�Ϊ-2�ۣ����ݻ������и�Ԫ�ػ��ϼ۴�����Ϊ�㣬̼�Ļ��ϼ۷ֱ�Ϊ��+2�� +4��
��4��d����Ԫ�أ����ݺ�������Ų����ɿ�֪����1����2�����ӣ���2����6�����ӣ���ԭ�ӽṹʾ��ͼΪ�� ��
��
��5���ڿ����е�ȼ��������ˮ����ѧ����ʽΪ��2H2 + O2![]() 2H2O��
2H2O��
��6������ϡ������Һ��Ӧ�����Ȼ�������������ѧ����ʽΪ��2Al + 6HCl = 2AlCl3 + 3H2����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ��ʵ���Ҳ���װ����ͼ��ʾ����ش��������⣮

��1��ѡ�������ռ�������װ�û�ҩƷ����д���±��У�����ĸ����
ѡ��ҩƷ | ����װ�� | �ռ�װ�� |
_____ | B | _____ |
������� | _____ |
��2������ö���������Ũ�����Ʊ���������ѡ�õķ���װ����_____ ������ĸ����
��3��ѡ��Fװ���ռ�����ʱ������ʵ�������ȷ����_____ ������ţ���
�ٷ�Ӧǰ��������ƿע��ˮ���ò���Ƭ��סƿ�ڣ�������ʢˮ��ˮ����
�ڿ�ʼ��Ӧ�ȵ����������Ҿ���ʱ���ٽ����ܿ����뼯��ƿ
���ռ����������ƿ��ˮ�¸��ϲ���Ƭ���Ƴ�ˮ��
��ʵ�����ʱ���ȳ��߾ƾ��ƣ�Ȼ���ܴ�ˮ����ȡ��
��4����Bװ����ȡ����ʱ����Ӧ���ʱȽϿ죬���ܵ���ʵ���ò���ȫ���������õĸĽ���ʩ��_____��