题目内容
(2009?广元)下图是实验室制取气体的一些装置,据图回答有关问题.
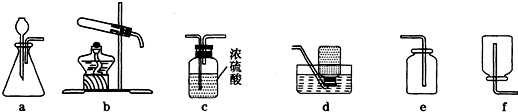
(1)写出实验室由装置a、e组合制取一种气体的化学方程式
(2)实验室用加热氯化铵和氢氧化钙两种固体混合物的方法来制取氨气(反应的化学方程式为:
2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑),选用的发生装置为
(3)氨气是一种密度比空气小、无色、有刺激性气味、极易溶于水的气体.氨气溶于水所得的溶液叫氨水,氨水显碱性.在实验室如果要制得干燥的氨气

(1)写出实验室由装置a、e组合制取一种气体的化学方程式
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
(2)实验室用加热氯化铵和氢氧化钙两种固体混合物的方法来制取氨气(反应的化学方程式为:
2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑),选用的发生装置为
b
b
.从制取氨气的反应原理可知铵态氮肥不能与碱性物质或氢氧化钙或草木灰等
不能与碱性物质或氢氧化钙或草木灰等
混合使用或存放.(3)氨气是一种密度比空气小、无色、有刺激性气味、极易溶于水的气体.氨气溶于水所得的溶液叫氨水,氨水显碱性.在实验室如果要制得干燥的氨气
不能
不能
(填“能”或“不能”)用装置C干燥气体.分析:(1)根据图中A、C装置的组合,分析可以制取的气体的反应物的状态及反应条件,气体的性质和收集方法,选择药品书写制取气体化学方程式;
(2)根据反应物的状态和反应条件确定实验室制取氨气的发生装置;根据制取氨气的反应原理分析铵盐的性质,总结铵盐的使用和存放方法;
(3)根据氨气的性质分析能否用装置C干燥的原因.
(2)根据反应物的状态和反应条件确定实验室制取氨气的发生装置;根据制取氨气的反应原理分析铵盐的性质,总结铵盐的使用和存放方法;
(3)根据氨气的性质分析能否用装置C干燥的原因.
解答:解:(1)由题意知:图中A、C装置的组合可以制取的一种气体,反应属于固液反应不需加热,收集的气体密度比空气大,用该装置可通过大理石和盐酸反应来制取二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)实验室用加热氯化铵和氢氧化钙两种固体混合物的方法来制取氨气,反应物的状态为固体,反应条件是加热,故可选用的发生装置是b;根据制取氨气的反应原理可知,铵盐能与碱反应放出氨气,所以,铵态氮肥不能与碱性物质或氢氧化钙或草木灰等混合使用或存放;
(3)由题意可知,氨气溶于水所得的溶液叫氨水,氨水显碱性,能与酸反应,所以,如果要制得干燥的氨气不能用浓硫酸来干燥,即不能用装置C干燥氨气.
故答为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑(2)b,不能与碱性物质或氢氧化钙或草木灰等;(3)不能.
(2)实验室用加热氯化铵和氢氧化钙两种固体混合物的方法来制取氨气,反应物的状态为固体,反应条件是加热,故可选用的发生装置是b;根据制取氨气的反应原理可知,铵盐能与碱反应放出氨气,所以,铵态氮肥不能与碱性物质或氢氧化钙或草木灰等混合使用或存放;
(3)由题意可知,氨气溶于水所得的溶液叫氨水,氨水显碱性,能与酸反应,所以,如果要制得干燥的氨气不能用浓硫酸来干燥,即不能用装置C干燥氨气.
故答为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑(2)b,不能与碱性物质或氢氧化钙或草木灰等;(3)不能.
点评:本题主要考查了气体制取装置的选择和连接方法,会根据气体的制取原理来组装、选配、判断或者选择气体的发生装置;再根据气体的溶解性、密度及其是否与水或者空气发生反应等来判断、选用收集装置.

练习册系列答案
相关题目
 (2009?广元)某学生为测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已略去),实验在
(2009?广元)某学生为测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已略去),实验在