题目内容
【题目】向27.4g含有氯化镁和碳酸镁的混合物中滴加盐酸,至无气泡产生,共用去10%的稀盐酸73g.试计算:
(1)原混合物中碳酸镁的质量分数.
(2)所得溶液中氯化镁的质量分数.
【答案】(1)30.7%;(2)29.7%.
【解析】试题分析:(1)根据碳酸镁和盐酸反应生成二氧化碳、氯化镁、水,依据盐酸的质量进行计算;
(2)根据化学方程式计算反应后溶液质量和溶质质量,然后计算溶质质量分数.
解:(1)设参加反应的碳酸镁的质量为x,生成氯化镁质量为y,生成二氧化碳质量为z
MgCO3+2HCl = MgCl2+H2O+CO2↑
84 73 95 44
x 10%×73g y z
![]() =
=![]() =
=![]() =
=![]()
x=8.4g
y=9.5g
z=4.4g
所以原混合物中碳酸镁的质量分数为:![]() ×100%=30.7%;
×100%=30.7%;
(2)所得溶液中氯化镁的质量分数为:![]() ×100%=29.7%.
×100%=29.7%.
故答案为:(1)30.7%;(2)29.7%.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
【题目】实验是科学探究的重要方法,如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题.
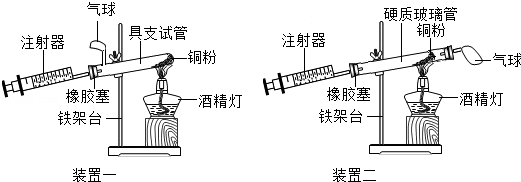
(1)根据下表提供的实验数据,完成下表.
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
25mL | 15mL | 9mL |
(2)装置一和装置二中气球的位置不同, (填“装置一”或“装置二”)更合理,理由是 .
(3)若实验测得的结果偏小(氧气的体积分数小于21%),可能的原因有哪些?(列举两条) 、 .