题目内容
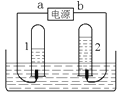
【题目】某同学模仿物理课上学到的“串联电路”,设计了如下气体制取与性质验证的组合实验。打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中。请看图回答问题:
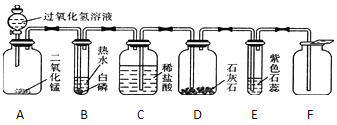
(1)A中发生反应的化学方程式为__________________________________________;
(2)B中白磷能够燃烧的原因是①白磷是可燃物,②温度达到了白磷的着火点,③_____________________________________________;
(3)D中发生反应的化学方程式为_______________________________。
(4)E中的实验现象是_____________________,E中反应的化学方程式为________________________。
(5)用F装置收集气体的依据是_______________________________。
(6)检验F装置集气瓶中含有二氧化碳的方法是__________________该反应的化学方程式为_____________________。
【答案】 2H2O2 ![]() 2H2O+ O2↑ 白磷与氧气接触 CaCO3 + 2HCl ===CaCl2 + H2O + CO2↑ 溶液由紫色变红色 H2O +CO2 =H2CO3 气体的密度比空气密度大 倒入澄清石灰水,石灰水变浑浊 CO2+Ca(OH)2===CaCO3↓+H2O
2H2O+ O2↑ 白磷与氧气接触 CaCO3 + 2HCl ===CaCl2 + H2O + CO2↑ 溶液由紫色变红色 H2O +CO2 =H2CO3 气体的密度比空气密度大 倒入澄清石灰水,石灰水变浑浊 CO2+Ca(OH)2===CaCO3↓+H2O
【解析】(1)过氧化氢在二氧化锰的催化作用下,生成水和氢气,化学反应方程式为: ![]()
![]()
![]() ;②B中白磷能够燃烧的原因是:白磷是可燃物;与氧气接触;温度达到着火点;(3)B中剩余氧气进入C装置,随着气体的增多,迫使稀盐酸进入D,盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,反应的化学方程式为:
;②B中白磷能够燃烧的原因是:白磷是可燃物;与氧气接触;温度达到着火点;(3)B中剩余氧气进入C装置,随着气体的增多,迫使稀盐酸进入D,盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,反应的化学方程式为: ![]() ;(4)氧气流进入C,则把盐酸压入D和石灰石反应生成二氧化碳,二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色,反应的化学方程式为:
;(4)氧气流进入C,则把盐酸压入D和石灰石反应生成二氧化碳,二氧化碳气体进入E,与水反应生成碳酸,紫色石蕊遇酸变红色,反应的化学方程式为: ![]() ;(5)二氧化碳气体的密度大于空气的密度,所以可用向上排空气法收集;⑥二氧化碳能使澄清石灰水变浑浊,所以检验二氧化碳可倒入澄清石灰水,该反应的化学方程式:
;(5)二氧化碳气体的密度大于空气的密度,所以可用向上排空气法收集;⑥二氧化碳能使澄清石灰水变浑浊,所以检验二氧化碳可倒入澄清石灰水,该反应的化学方程式: ![]() 。
。

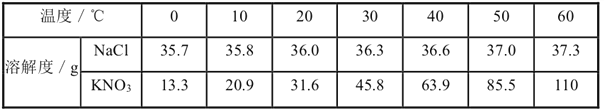
【题目】下表列出了固体物质A在不同温度时的溶解度:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 36 | 35 | 34 | 33 | 32 | 31 | 30 | 29 | 28 | 27 |
(1)70℃时,向盛有100g水的烧杯中加入30g固体A,充分溶解形成的是______________(填“饱和”或“不饱和”)溶液,再将烧杯内物质温度降至20℃,此时溶液中溶质与溶剂的质量比为_____________(填最简整数比);
(2)通过对上表数据的分析,物质A的溶解度曲线应是右图中的___________(填“甲”或“乙”);

(3)80℃时,配制一定量A物质的溶液,将其降温到60℃,是否有固体析出?____________(填“有”、 “没有”或“不确定”)。