题目内容
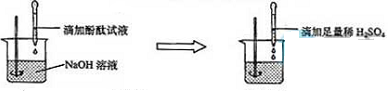
物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变呢?甲、乙两位同学按下面的步骤进行探究:
(1)提出假设:物质发生化学变化前后总质量不变。
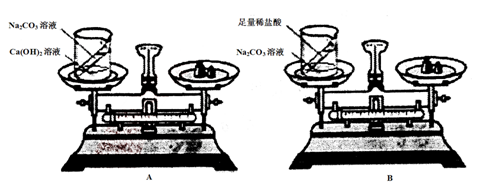
(2)进行实验:甲同学设计的实验装置和选用药品如图A所示,乙设计的实验装置和选用药品如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。
写出A、B两个实验发生反应的化学方程式:A、
B、 。
(3)实验结论:
甲认为:在化学反应中,生成物的总质量与反应物的总质量相等;
乙认为:在化学反应中,生成物的总质量与反应物的总质量不相等。
你认为导致乙同学实验结论错误的原因什么?

(1)提出假设:物质发生化学变化前后总质量不变。
(2)进行实验:甲同学设计的实验装置和选用药品如图A所示,乙设计的实验装置和选用药品如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。
写出A、B两个实验发生反应的化学方程式:A、
B、 。
(3)实验结论:
甲认为:在化学反应中,生成物的总质量与反应物的总质量相等;
乙认为:在化学反应中,生成物的总质量与反应物的总质量不相等。
你认为导致乙同学实验结论错误的原因什么?
(2)①Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
②Na2CO3+2HCl=2NaCl+H2O+CO2↑
(4)乙同学未考虑生成的气体逸散到空气中的质量。
②Na2CO3+2HCl=2NaCl+H2O+CO2↑
(4)乙同学未考虑生成的气体逸散到空气中的质量。
本题考查的是质量守恒定律的实验探究。
(2)书写化学方程式时要注意反应物和生成物的化学式,并且不要忘记配平和生成物状态符号。
A、碳酸钠和氢氧化钙反应,生成碳酸钙沉淀和氢氧化钠,故反应的化学方程式为:
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
B、碳酸钠和盐酸反应,生成氯化钠、水和二氧化碳,故反应的化学方程式为:
Na2CO3+2HCl=2NaCl+H2O+CO2↑
(3)因为在质量守恒定律中,反应物的总质量等于生成物的总质量,乙同学的实验漏掉生成物的气体的质量;故在表达质量守恒定律时,一定不要漏掉反应物或生成物的质量,特别是气体物质,容易忽略。
(2)书写化学方程式时要注意反应物和生成物的化学式,并且不要忘记配平和生成物状态符号。
A、碳酸钠和氢氧化钙反应,生成碳酸钙沉淀和氢氧化钠,故反应的化学方程式为:
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
B、碳酸钠和盐酸反应,生成氯化钠、水和二氧化碳,故反应的化学方程式为:
Na2CO3+2HCl=2NaCl+H2O+CO2↑
(3)因为在质量守恒定律中,反应物的总质量等于生成物的总质量,乙同学的实验漏掉生成物的气体的质量;故在表达质量守恒定律时,一定不要漏掉反应物或生成物的质量,特别是气体物质,容易忽略。

练习册系列答案
相关题目