��Ŀ����
����Ŀ���Ͼɽ������Ի������ã��úϽ���ϣ���Fe��Cu��Al����ȡFeSO4��Һ�ͻ��ս���Cu��ʵ��������ͼ��ʾ���������������ԣ��� 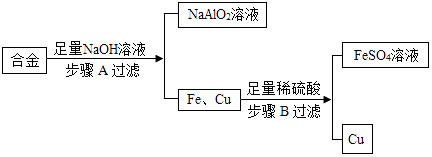
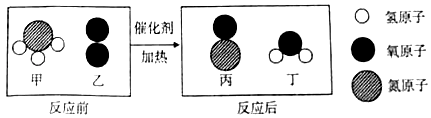
��1���Ͻ���������������������
��2������������������ʴ��ԭ�����û�ѧ��Ӧ����ʽ���ͣ���
��3������A��ѧ��Ӧ����ʽ��ʾΪ��2Al+2NaOH+2R�T2NaAlO2+3H2�������������غ㶨���Ƴ�R�Ļ�ѧʽΪ ��
��4������B�����Ļ�ѧ����ʽΪ����Ӧ�Ļ�������Ϊ ��
���𰸡�
��1�������
��2��4Al+3O2=2Al2O3
��3��H2O
��4��Fe+H2SO4=FeSO4+H2�����û���Ӧ
���������⣺��1���Ͻ��ǽ����ͽ����������ͷǽ��������ۺϵõ��ģ�������������ֻ����������ɵģ����ԺϽ����ڻ�����2������������Ӧ��������������ѧ����ʽΪ��4Al+3O2=2Al2O3����3������������2����ԭ�ӣ�2����ԭ�ӣ�4����ԭ�ӣ�6����ԭ�ӣ���Ӧ������2����ԭ�ӣ�2����ԭ�ӡ���ԭ�ӡ���ԭ�ӣ�����R��H2O����4������ϡ���ᷴӦ����������������������ѧ����ʽΪ��Fe+H2SO4=FeSO4+H2�����÷�Ӧ�����û���Ӧ�� �ʴ�Ϊ����1��������2��4Al+3O2=2Al2O3����3��H2O����4��Fe+H2SO4=FeSO4+H2�����û���Ӧ��
��1�����ݺϽ�Ķ���ͻ����Ķ�����з�������2����������������Ӧ�������������з�������3�����ݻ�ѧ��Ӧǰ��ԭ�Ӹ���������з�������4�������������ᷴӦ���������������������з�����

 ������ȫ�̼����ĩ���100��ϵ�д�
������ȫ�̼����ĩ���100��ϵ�д�