题目内容
【题目】每年3月22日是“世界水日”。水与人类的生活和生产密切相关。
(1)为了探究“水的净化”过程,我校化学实验小组从鸭绿江中取了水样,观察到水样呈黄绿色,有异味,且水样浑浊,有固体小颗粒。现对水样进行如下处理:
①向水样中加入明矾,充分搅拌,明矾的作用是_____;
②之后还要向得到的液体中加入_____,除去水样中的颜色和异味;
③小组同学利用一种新型的自来水消毒剂X,对水进行消毒。工业上制取X 的化学方程式为:Cl2 + 2 NaClO2 =2 NaCl + 2 X,则X的化学式为_____;
④天然水净化处理后要降低其硬度,采用的最简单的方法是_____。
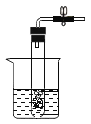
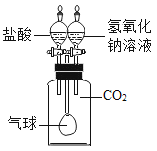
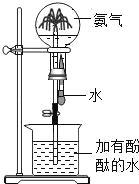
(2)同学们又在实验室进行如下图所示的实验,此实验中a管产生的气体能_____; 若a与b试管内收集的气体体积比大于2:1的原因_____。

(3)在验证了两集气管的产物之后小组成员又画出了该反应的微观示意图如下图,分别用“![]() ”和“
”和“![]() ”表示氧原子和氢原子。
”表示氧原子和氢原子。

小明同学认为反应前方框内应再填入一个粒子,请从下列A、B、C三个图示中选出_____,小明做出此判断的理论依据是_____。
A ![]() B
B ![]() C
C ![]()
【答案】吸附杂质,使之沉降 活性炭 ClO2 煮沸 能燃烧(或能被点燃) O2比H2易溶于水(或O2与电极发生反应了) C 质量守恒定律
【解析】
(1)①向水样中加入明矾,充分搅拌,明矾的作用是吸附杂质,使之沉降;
②之后还要向得到的液体中加入活性炭,除去水样中的颜色和异味;
③根据![]() 和质量守恒定律可知,2X含有2Cl、4O,则X的化学式为
和质量守恒定律可知,2X含有2Cl、4O,则X的化学式为![]() ;
;
④降水煮沸可以使钙镁离子沉淀,天然水净化处理后要降低其硬度,采用的最简单的方法是煮沸。
(2)该实验为电解水的实验,水通电时,正极产生氧气,负极产生氢气,体积比为2:1 ,a管产生的气体为氧气,能燃烧; 若a与b试管内收集的气体体积比大于2:1,原因是O2比H2易溶于水(或O2与电极发生反应了)
(3)根据水电解反应生成氢气和氧气的化学方程式: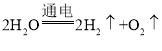 可知,应填入的粒子为水分子
可知,应填入的粒子为水分子![]() ,故填C;判断的理论依据是质量守恒定律。
,故填C;判断的理论依据是质量守恒定律。