��Ŀ����
����Ŀ���������ͼ�ش����⡣
A B
B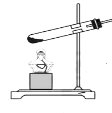 C
C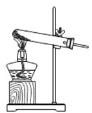 D
D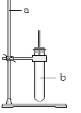
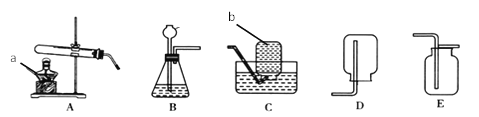
��1��д��ָ������������: a ____��b ____��
��2����ͬѧ���� KClO3 �� MnO2 ��ȡ O2������װ��Ӧѡ_____����ĸ�����÷�����ȡ O2��ѧ����ʽ _____�����ڵĻ�����Ӧ����Ϊ_____��Ӧ��
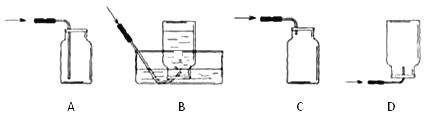
��3����ͬѧ���ռ��õ�����֮����Ӧ������ƿ_____�������������������������� ������
��4��þ��һ�ֻ�ѧ���ʻ��õĽ��������ڿ������ܱ���ȼ����ѧ����ʽ��________��
��5����ҵ�ϲ�ȡ������Һ���ٷ��뵪���ķ�����ȡ��������������Ĺ������� ____������������������ѧ�����仯��
��6����ͬѧ��ȱ�� MnO2 ����������������� KMnO4 ��϶�� KClO3 �������������ȡ�������÷����Ƿ����____����������������������������������____��
���𰸡�����̨ �Թ� B 2KClO3![]() 2KCl+3O2�� �ֽ� ���� 2Mg+O2
2KCl+3O2�� �ֽ� ���� 2Mg+O2![]() 2MgO ���� ���� ��������ڼ��ȵ����������ɵĶ������̿��Դ�����صķֽ�
2MgO ���� ���� ��������ڼ��ȵ����������ɵĶ������̿��Դ�����صķֽ�
��������
��1��ͨ������������ָ���������ƺ����ÿ�֪��a������̨��b���Թܣ�
��2��ʵ�������������ȡ�����ķ�Ӧ���ǹ��壬��Ӧ�����Ǽ��ȣ���������KClO3��MnO2��ȡO2������װ��ӦѡB��������ڶ������̵Ĵ������¼��������Ȼ��غ���������ѧ����ʽΪ��2KClO3![]() 2KCl+3O2�����÷�Ӧ���ڷֽⷴӦ��
2KCl+3O2�����÷�Ӧ���ڷֽⷴӦ��
��3�������ܶȱȿ������������ռ��õ�����֮��Ӧ������ƿ���������ϣ�
��4��þ�������ڵ�ȼ����������������þ����ѧ����ʽΪ��2Mg+O2![]() 2MgO��
2MgO��
��5����ҵ�ϲ�ȡ������Һ���ٷ��뵪���ķ�����ȡ����û�����������ɣ����������仯��
��6����������ڼ��ȵ���������������ء��������̺����������ɵĶ������̿��Դ�����صķֽ⣬���Ը÷������С�

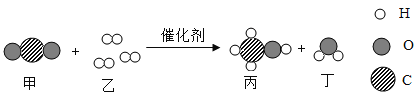
����Ŀ��������һ������������ȼ�գ���÷�Ӧǰ������ʵ��������±���ʾ��
���� | ���� | ���� | ˮ | ������̼ | X |
��Ӧǰ����/g | 3.2 | 11.2 | 0 | 0 | 0 |
��Ӧ������/g | 0 | 0 | 7.2 | 4.4 | a |
�����ж���ȷ����
A������a��ֵΪ2.6 B��Xһ���Ǹ÷�Ӧ�Ĵ���
C��X���ܺ�����Ԫ�� D��Xһ��������Ԫ��