题目内容
海洋为人类提供了宝贵的自然资源.
(1)食用海鱼摄取的主要营养素是 .
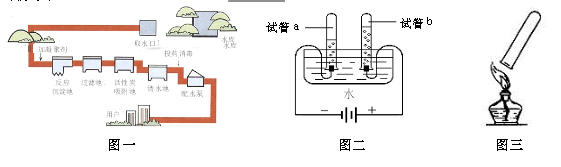
(2)下图为海水淡化装置,利用的能源是 ,获得的蒸馏水属于 (填字母序号).

A.单质 B.化合物 C.混合物
(3)从海水中提取食盐,采用的方法是 .
(4)用氯化钠和碳酸氢铵(NH4HCO3)可制备碳酸氢钠和氯化铵(NH4Cl),该反应可表示为:NaCl+NH4HCO3═NaHCO3+NH4Cl.
20℃时,按上述化学方程式中反应物的质量比,向100g水中加入11.7g NaCl和15.8g NH4HCO3.理论上从溶液中析出晶体的质量为 g.
资料:20℃时四种物质的溶解度如下,假设它们同时溶解在水中各自的溶解度不变.
(1)食用海鱼摄取的主要营养素是 .
(2)下图为海水淡化装置,利用的能源是 ,获得的蒸馏水属于 (填字母序号).

A.单质 B.化合物 C.混合物
(3)从海水中提取食盐,采用的方法是 .
(4)用氯化钠和碳酸氢铵(NH4HCO3)可制备碳酸氢钠和氯化铵(NH4Cl),该反应可表示为:NaCl+NH4HCO3═NaHCO3+NH4Cl.
20℃时,按上述化学方程式中反应物的质量比,向100g水中加入11.7g NaCl和15.8g NH4HCO3.理论上从溶液中析出晶体的质量为 g.
资料:20℃时四种物质的溶解度如下,假设它们同时溶解在水中各自的溶解度不变.
| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 |
| 溶液度/g | 36.0 | 21.6 | 37.2 | 9.6 |
(1)蛋白质;(2)太阳能;B;(3)蒸发结晶;(4)7.2g
(1)鱼类中含有较多的蛋白质,所以食用海鱼摄取的主要营养素是蛋白质;
(2)从图中可以得出使用的为太阳能;而得到的蒸馏水为纯净物,故选B;
(3)海水晒盐是将海水中过多的水分蒸发,而得到食盐晶体的过程,所以其原理为蒸发结晶;
(4)解:根据化学方程式中质量关系可以知道:
NaCl+NH4HCO3═NaHCO3+NH4Cl
58.5 79 84 53.5
11.7g 15.8g 16.8g 10.7g
满足化学式中相对分子质量的关系,故可以知道可以得到碳酸氢钠的质量为16.8g,生成氯化铵的质量为10.7g,根据题中的溶解度表可以知道,20℃时 100g水中能够溶解碳酸氢钠的质量为9.6g,能够溶解氯化铵的质量为37.2g,所以能够析出的晶体的质量为16.8g-9.6g=7.2g
(2)从图中可以得出使用的为太阳能;而得到的蒸馏水为纯净物,故选B;
(3)海水晒盐是将海水中过多的水分蒸发,而得到食盐晶体的过程,所以其原理为蒸发结晶;
(4)解:根据化学方程式中质量关系可以知道:
NaCl+NH4HCO3═NaHCO3+NH4Cl
58.5 79 84 53.5
11.7g 15.8g 16.8g 10.7g
满足化学式中相对分子质量的关系,故可以知道可以得到碳酸氢钠的质量为16.8g,生成氯化铵的质量为10.7g,根据题中的溶解度表可以知道,20℃时 100g水中能够溶解碳酸氢钠的质量为9.6g,能够溶解氯化铵的质量为37.2g,所以能够析出的晶体的质量为16.8g-9.6g=7.2g

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目