题目内容
(2011?攀枝花)碳酸氢钠常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的热稳定性进行探究.【查阅资料】
1.碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种______常见的固体物质.
2.碳酸钠溶液呈碱性.
【进行实验】
为了验证碳酸氢钠受热时会分解,兴趣小组的同学取一定质量的碳酸氢钠到铜片上加热,如右上图所示.
(1)加热一段时间后,观察到烧杯内壁有______.
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊.写出该反应的化学方程式:______.
(3)兴趣小组的同学认为:充分加热后的固体产物可能是NaOH或Na2CO3.
①他们的依据是______.
②兴趣小组为了确定反应后的固体产物成分进行以下实验,请填写下表:
| 实验 | 实验现象 | 结论 |
| 实验一:取少量反应后的固体产物溶于水,滴入几滴酚酞试液 | 溶液变成红色 | 固体产物是NaOH,而不是Na2CO3 |
| 实验二:取少量反应后的固体产物溶于水,加入过量氯化钙溶液 | ______ | 固体产物是Na2CO3,而不是NaOH |
| 实验三:______ | 产生大量气泡 | 固体产物是Na2CO3,而不是NaOH |
【总结】请写出碳酸氢钠受热分解的化学方程式______ Na2CO3+CO2↑+H2O

【答案】分析:实验部分由于已经假设了加热后的固体产物是NaOH或Na2CO3,所以应分析下面肯定是要利用NaOH和Na2CO3性质的不同点来设计实验,才能得到正确结论.而不能用NaOH和Na2CO3的共同性质来设计实验,如NaOH和Na2CO3溶液都呈碱性,所以不能用滴酚酞试液来设计实验.
解答:解:(1)因为已经知道碳酸氢钠受热分解时有水生成,所以加热一段时间后,倒扣的烧杯内壁有水珠出现;
(2)二氧化碳使澄清石灰水变浑浊的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O
(3)①根据质量守恒定律可知化学反应前后元素种类不变,因为NaHCO3中含有Na、H、C、O元素,所以兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3.
②实验二:取少量反应后的固体产物溶于水,加入过量氯化钙溶液,因为NaOH和Na2CO3中只Na2CO3有和氯化钙溶液反应生成白色沉淀,所以实验现象为:产生白色沉淀;实验三的实验现象是产生大量气泡,而NaOH和Na2CO3中只有Na2CO3和酸反应会产生二氧化碳气体,所以实验步骤为:取少量反应后的固体产物,加入过量稀盐酸.
【讨论与评价】实验一的结论明显是不正确的,因为NaOH和Na2CO3的溶液都显碱性,都能使滴酚酞试液变红.
【总结】通过实验二和实验三可知碳酸氢钠受热分解后的固体产物是Na2CO3,所以碳酸氢钠受热分解的化学方程式为:2NaHCO3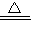 Na2CO3+CO2↑+H2O.
Na2CO3+CO2↑+H2O.
故答案为:(1)水珠(或水雾等)
(2)Ca(OH)2+CO2=CaCO3↓+H2O
(3)①质量守恒定律(或化学反应前后元素种类不变或化学反应前后原子种类不变或NaHCO3中含有Na、H、C、O元素)
②
【讨论与评价】碳酸钠溶液呈碱性,也能使无色酚酞变成红色
【总结】2NaHCO3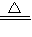 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
点评:此题是一道实验设计题,因为此题已经给出了碳酸氢钠受热分解后的固体产物可能是NaOH或Na2CO3,不用学生探究碳酸氢钠受热分解后的固体是什么,使此题的难度有所降低.另外此题也很好的考查了学生们对重要化学方程式的记忆.
解答:解:(1)因为已经知道碳酸氢钠受热分解时有水生成,所以加热一段时间后,倒扣的烧杯内壁有水珠出现;
(2)二氧化碳使澄清石灰水变浑浊的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O
(3)①根据质量守恒定律可知化学反应前后元素种类不变,因为NaHCO3中含有Na、H、C、O元素,所以兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3.
②实验二:取少量反应后的固体产物溶于水,加入过量氯化钙溶液,因为NaOH和Na2CO3中只Na2CO3有和氯化钙溶液反应生成白色沉淀,所以实验现象为:产生白色沉淀;实验三的实验现象是产生大量气泡,而NaOH和Na2CO3中只有Na2CO3和酸反应会产生二氧化碳气体,所以实验步骤为:取少量反应后的固体产物,加入过量稀盐酸.
【讨论与评价】实验一的结论明显是不正确的,因为NaOH和Na2CO3的溶液都显碱性,都能使滴酚酞试液变红.
【总结】通过实验二和实验三可知碳酸氢钠受热分解后的固体产物是Na2CO3,所以碳酸氢钠受热分解的化学方程式为:2NaHCO3
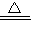 Na2CO3+CO2↑+H2O.
Na2CO3+CO2↑+H2O.故答案为:(1)水珠(或水雾等)
(2)Ca(OH)2+CO2=CaCO3↓+H2O
(3)①质量守恒定律(或化学反应前后元素种类不变或化学反应前后原子种类不变或NaHCO3中含有Na、H、C、O元素)
②
| 实验 | 实验现象 |
| 方案二: | 产生白色沉淀 |
| 方案三:取少量反应后的固体产物,加入过量稀盐酸(或稀硫酸、稀硝酸、醋酸) |
【总结】2NaHCO3
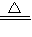 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O点评:此题是一道实验设计题,因为此题已经给出了碳酸氢钠受热分解后的固体产物可能是NaOH或Na2CO3,不用学生探究碳酸氢钠受热分解后的固体是什么,使此题的难度有所降低.另外此题也很好的考查了学生们对重要化学方程式的记忆.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
 ,氯原子的最外层电子数为.下列图中微粒共表示种元素,其中与氯原子具有相似化学性质的是(填序号).
,氯原子的最外层电子数为.下列图中微粒共表示种元素,其中与氯原子具有相似化学性质的是(填序号).
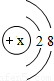 ,则x的数值可能是下列中的.
,则x的数值可能是下列中的.