题目内容
【题目】取氯酸钾和二氧化锰的混合物12克制取氧气,加热一段时间后,测得50%的氯酸钾分解,将剩余的固体冷却后称量,其质量为10.08克。
(1)二氧化锰是该反应的_____________剂;氯酸钾中氯元素的化合价为:__________。
(2)反应生成的氧气的质量为___________?
(3)原混合物中氯酸钾的质量为___________?
【答案】 催化 +5 1.92 g 9.8 g
【解析】(1)氯酸钾在二氧化锰的催化下加热分解产生氯化钾和氧气,二氧化锰改变了化学反应的速率,但自身的质量和化学性质在反应前后不变,二氧化锰是该反应的催化剂,氯酸钾中氧元素显-2价,钾元素显1价,设氯元素的化合价为x,则有(+1)+x+(-2)X3=0,x=+5,即氯元素的化合价为+5;(2) 根据质量守恒定律,反应生成氧气的质量为
12g-10.08g- 1.92g;(3) 设已分解的氯酸钾质量为![]() ,
,
2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
245 96
![]() 1.92g
1.92g
![]()
原混合物中氯酸钾的质量为:4.9g![]() 50%=9.8g。
50%=9.8g。
答:二氧化锰是该反应的催化剂,氯酸钾中氯元素的化合价为:+5价,反应生成氧气的质量为1.92g,原混合物中氯酸钾的质量为9.8g。

 阅读快车系列答案
阅读快车系列答案【题目】实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程:____________________________。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(℃) |
① | KClO3 | 580 |
② | KClO3、MnO2(质量比1:1) | 350 |
③ | KClO3、CuO(质量比1:1) | 370 |
④ | KClO3、Fe2O3(质量比1:1) | 390 |
【分析数据、得出结论】(1)由实验_______与实验4对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是_________________。
【反思】(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的_______和_________不变;
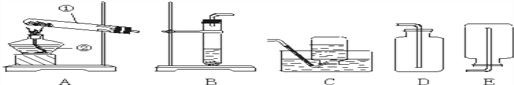
(2)画图(在下面空白处画出实验室高锰酸钾制取并收集氧气的装置图)_____________。
(3)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可)________________。
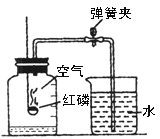
【题目】(1)下图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中不正确的是 (_________)
A.集气瓶内加入少量水可防止瓶底炸裂
B.该实验所用红磷的量不足可能造成气体减少的体积小于五分之一
C.实验时,点燃的红磷要立即伸入集气瓶中,并塞紧橡皮塞
D.红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹
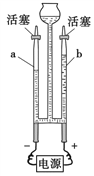
(2)研究性学习小组的同学为探究空气中氧气的体积分数,设计了如下图所示装置。请根据图示实验回答下列问题:
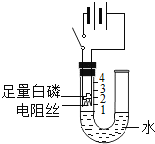
①闭合电源开关,可以观察到白磷_______________________________。
②装置冷却到室温,可观察到U型管内左侧液面______________________。
③通过这个实验得出的结论是_________________________。
④此实验还可推知反应后剩余气体的两点性质是:______________;_____________。
(3)如下图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行试验。请完成实验报告:(40℃以上白磷就开始燃烧)
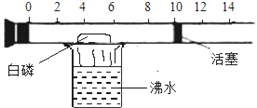
实验目的 | 实验现象 | 实验结论 |
测定空气中____的 体积分数。 | 白磷着火燃烧,活塞先右移, 后左移,最后停在刻度约为_____(填整数)的位置上。 | 空气的成分按体积计算, 氧气约占______。 |