题目内容
【题目】实验是化学灵魂,是学好化学的重要环节。
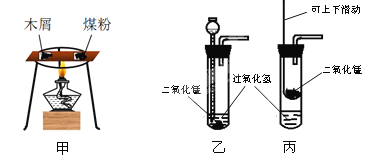
(1)《燃烧的条件》实验中,分别取适量木屑和煤粉(同样大小),分开放在一块薄铜片的两侧如图甲所示,加热铜片的中部,观察到的现象是 ;该实验说明_________________。
(2)装置乙、丙分别是实验室制取氧气的发生装置(夹持仪器略),两种发生装置比较 (填编号)更好,原因是 。
【答案】(1)木屑先燃烧,煤粉后燃烧;说明着火点低的可燃物易燃烧,着火点高的可燃物不易燃烧(合理即可)(2)乙 乙装置能得到稳定的气流(合理即可)
【解析】
试题分析:(1)用棉花分别蘸酒精和水,放在酒精灯外焰上加热.该实验的目的是探究可燃物是燃烧的条件之一,该实验的可燃物是指酒精,实验成功的关键之一是控制棉花不燃烧.(2)乙装置中二氧化锰是否与过氧化氢溶液接触是可控的,这样就能控制反应的速率。

【题目】善于梳理化学知识,能使你的头脑更聪明。以下知识的梳理有错误的一组是
A.[性质与用途] ①CO具有还原性--用于冶炼金属 ②石墨具有导电性--作电极 | B.[物质的分类] 由多种物质组成--混合物 含有氧元素的化合物--氧化物 |
C.[安全知识] ①碰倒酒精灯致洒出的酒精在桌上燃烧--立即用湿布盖灭 ②皮肤上不慎沾上氢氧化钠溶液--用大量的水冲洗,再涂上硼酸溶液 | D.[生活经验] ①区分白酒和白醋--闻气味 ②刚装修好的房间不易立即入住--会挥发出甲醛污染空气,应选择不含甲醛的绿色环保产品 |
【题目】某同学为测定实验室中某氯酸钾样品的纯度,取2.5g该样品与0.5g二氧化锰混合,加热该混合物t1时间后(杂质不参加反应),冷却,称量剩余固体质量,重复以下操作,依次称得加热t2、t3、t4时间后剩余固体的质量,记录数据如下表
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量(g) | 2.68 | 2.52 | 2.04 | 2.04 |
(1)加热至t3时间时,氯酸钾是否已经完全反应? (填“是”或“否”).
(2)完全反应后产生氧气的质量是 g.
(3)计算t2时刻,样品中有多少氯酸钾发生了分解?