题目内容
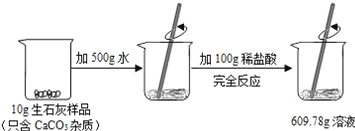
【题目】某石灰厂需要测定产品生石灰中杂质(杂质只含CaCO3)的质量分数.小刚进行了如图实验.请计算:
(1)生成CO2气体的质量;
(2)样品中CaCO3的质量分数.
【答案】0.22g.
@5%.
【解析】(1)反应前药品的总质量为500g+100g+10g=610g,反应后样品的总质量为609.78g ,根据质量守恒定律,生成二氧化碳的质量为:610g-609.78g=0.22g;
(2)设生成0.22g的二氧化碳气体需要碳酸钙的质量为x
CaCO3+2HCl == CaCl2+H2O+CO2↑
100 44
x 0.22g
![]() =
=![]() x=0.5g
x=0.5g
样品中CaCO3的质量分数=![]() =5%
=5%
答:生成二氧化碳的质量为0.22g,样品中碳酸钙的质量分数为5%。

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目