题目内容
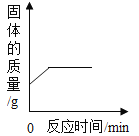
【题目】下列四个图象能正确反映对应变化关系的是( )
A.在密闭容器中用红磷测定空气中氧气的含量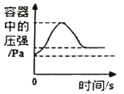
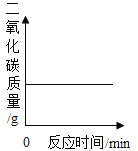
B.向盛有二氧化锰的烧杯中不断加入过氧化氢溶液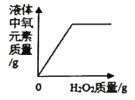
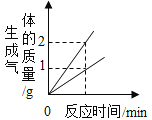
C.等质量氯酸钾制氧气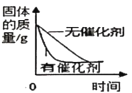
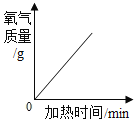
D.加热高锰酸钾制取氧气时剩余物的质量
【答案】D
【解析】
A、在密闭容器中用红磷燃烧测定空气中氧气的含量,氧气被消耗,最终装置内的压强将变小,故选项错误;
B、向盛有二氧化锰的烧杯中不断加入过氧化氢溶液,产生水和氧气,二氧化锰是该反应的催化剂,化学性质在反应后不变,加入过氧化氢溶液,液体中的氧元素的质量一直增大,故选项错误;
C、等质量氯酸钾制氧气,加入催化剂后,固体质量不相同,两者图像起点位置不同,故选项错误;
D、加热高锰酸钾制产生锰酸钾、二氧化锰和氧气,随反应的进行,剩余物的质量不断减少,反应结束后,固体质量不变,故选项正确。故选D。

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案【题目】某实验小组的同学为了测定实验室中高锰酸钾样品的纯度,取20g该样品,依次加热该混合物,t1、t2、t3、t4时间后,称得剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量(g) | 19.88 | 19.56 | 19.36 | 19.36 |
试计算:(1)加热__________时间后高锰酸钾已经完全反应。
(2)完全反应后产生氧气的质量为_________g。
(3)求该样品中高锰酸钾的质量分数_______。
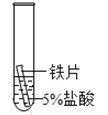
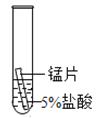
【题目】某研究小组为探究铁、铜、锰(Mn)、银的金属活动性顺序,进行了如下三个实验(其中金属均已打磨,且形状、大小相同,试管中所用溶液的体积相同)。下列判断不正确的是
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
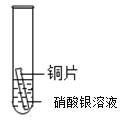
实验现象 | 立即产生气泡,速率较慢 | 立即产生气泡,速率较快 | 铜片的表面有银白色固体,一段时间后。溶液由无色变为蓝色 |
A.通过实验一和实验二的反 应剧烈程度,能判断出铁和锰的金属活动性强弱
B.在上述三个实验基础上再增加一个铜和5%盐酸的实验,则能判断出四种金属的活动性顺序
C.通过上述三个实验,能判断出四种金属的活动性顺序
D.通过实验三的反应现象,能判断出铜和银的金属活动性强弱
【题目】价类二维图反映的是元素化合价与物质类别之间的关系,构建价类二维图是化学学习的重要方法。下图是某同学绘制的关于碳元素的价类二维图。
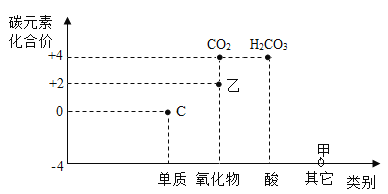
(1) 甲为天然气的主要成分,其化学式为_____。
(2) 根据碳元素的价类二维图完成下表:
物质之间的反应或转化 | 碳元素化合价的变化情况 | 化学方程式 |
CO2→H2CO3 | 不变 | ①_____ |
C→乙 | 升高 | ②_____ |
C和CO2反应 | ③_____ | C+ CO2 |
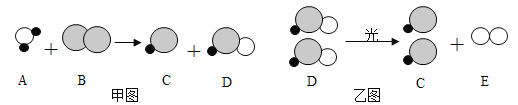
(3)以CO2为原料,与H2经催化可转化为A物质,反应原理如下图所示:
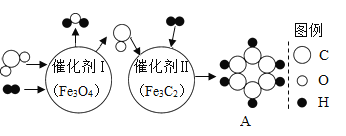
①写出A的化学式_____。
②在催化剂Ⅰ(Fe3O4)作用下发生反应的化学方程式为_____。
【题目】老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种。同学们对该粉末进行了研究。
(1)
实验方案 | 实验现象 | 实验结论 |
取少量红色粉末放入试管中,滴加足量的稀盐酸振荡 | 红色粉末全部消失,溶液呈棕黄色 | 粉末为Fe2O3 |
粉末为Cu |
写出“红色粉末全部消失”发生反应的化学方程式_______。
(2)取该粉末放入硬质玻璃管中,先通CO,然后再用酒精喷灯加热一段时间,停止加热继续通入CO至装置冷却。实验装置如图:
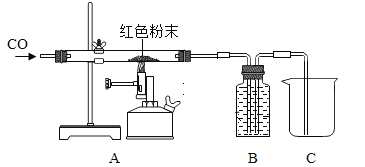
①实验时,先通CO再加热的目的是_________。
②若该粉末全部是氧化铁,在硬质玻璃管中观察到的实验现象是_________。B装置是用于吸收二氧化碳并收集CO,其中盛放的试剂最好是__________。
A NaOH 溶液 B 稀盐酸 C 水
③如果该实验没有装置B、C,实验造成的危害是_______。