题目内容
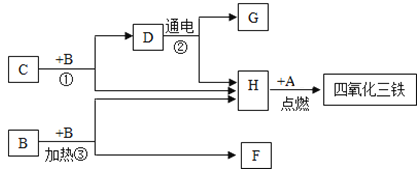
【题目】化学实验是进行科学探究的重要方式,思考下列问题并回答。
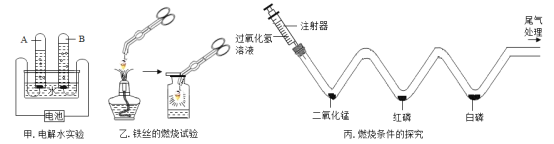
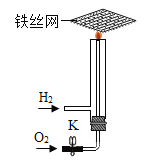
(1)实验甲中电源接通一段时间后,A管中产生气体为10 mL时,则B管中产生气体体积为___________mL,检验B管中生成的气体,可将__________伸入气体中。电解水时,向水中加入少量稀硫酸,目的是_____________。
(2)实验乙中,瓶底放少量水,目的是______________,若反应中没有看到“火星四射”的现象,可能的原因是______________(写一种即可)。
(3)实验丙中,将注射器中的溶液缓缓推入 V 形管,二氧化锰与过氧化氢溶液混合产生大量气泡,此处反应的化学方程式为_____________;用 80℃的热水加热盛有红磷和白磷的 W 形管时,发现白磷燃烧而红磷不燃烧,由此可说明燃烧需要的条件是___________ 。
(4)某兴趣小组依据教材实验对质量守恒定律进行了如下探究,根据下图回答问题:
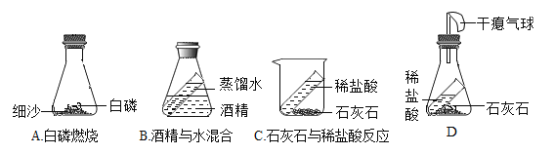
①如图 A、B、C三个实验装置(天平略),其中能用来验证质量守恒定律的是__________(填字母序号)。
②从微观角度解释反应前后质量守恒的原因是_________。
③小明将图 C 装置改进成如图 D 所示,装置气密性良好,但是反应后天平指针向右偏转,请解释原因___________。
【答案】5 带火星的木条 增强水的导电性 防止热的熔化物直接落到瓶底使瓶底炸裂 铁丝表面的铁锈未除去(合理即可) 2H2O2![]() 2H2O+O2↑ 温度要达到可燃物的着火点 A 在化学反应前后,原子的种类、个数与质量不变 稀盐酸和石灰石在密封容器中反应且生成的二氧化碳气体没有逸出,进入气球后使气球体积膨胀,所受到的浮力变大,所以称得的质量变小
2H2O+O2↑ 温度要达到可燃物的着火点 A 在化学反应前后,原子的种类、个数与质量不变 稀盐酸和石灰石在密封容器中反应且生成的二氧化碳气体没有逸出,进入气球后使气球体积膨胀,所受到的浮力变大,所以称得的质量变小
【解析】
(1)实验甲中电源接通一段时间后,A管中产生气体为10 mL时,则B管中产生气体体积为5mL,因为由图知B试管中的气体少为氧气,A试管中是氢气,且电解水时产生的氢气与氧气的体积比为2:1,由于B试管中是氧气,它具有助燃性,所以检验B管中生成的气体,可将带火星的木条伸入气体中,若木条复燃则为氧气。因为纯水的导电性弱,所以电解水时,向水中加入少量稀硫酸,目的是增强水的导电性,故填:5 带火星的木条 增强水的导电性。
(2)实验乙是铁丝在氧气中燃烧的实验,此反应是放热反应,所以在瓶底放少量水,目的是防止热的熔化物直接落到瓶底使瓶底炸裂,若反应中没有看到“火星四射”的现象,可能的原因是铁丝表面的铁锈未除去,因为若铁锈未除去则会阻碍铁丝在氧气中燃烧,故填:防止热的熔化物直接落到瓶底使瓶底炸裂 铁丝表面的铁锈未除去。
(3)实验丙中,将注射器中的溶液缓缓推入 V 形管,二氧化锰与过氧化氢溶液混合产生氧气和水,所以看到大量气泡,此处反应的化学方程式为2H2O2![]() 2H2O+O2↑;用 80℃的热水加热盛有红磷和白磷的 W 形管时,发现白磷燃烧而红磷不燃烧,由此可说明燃烧需要的条件是温度要达到可燃物的着火点,因为白磷的着火点是40℃而红磷的着火点为240℃,所以白磷燃烧而红磷不燃烧,故填:2H2O2
2H2O+O2↑;用 80℃的热水加热盛有红磷和白磷的 W 形管时,发现白磷燃烧而红磷不燃烧,由此可说明燃烧需要的条件是温度要达到可燃物的着火点,因为白磷的着火点是40℃而红磷的着火点为240℃,所以白磷燃烧而红磷不燃烧,故填:2H2O2![]() 2H2O+O2↑ 温度要达到可燃物的着火点。
2H2O+O2↑ 温度要达到可燃物的着火点。
(4)①图 A、B、C三个实验装置,其中能用来验证质量守恒定律的是A,A因为白磷燃烧发生了化学变化,且在密封容器中进行,所以反应前后质量守恒;B中没有发生化学变化;C不是密封容器,产生的二氧化碳不能被称量到,所以反应后天平称得的质量会比反应前少。
②从微观角度解释反应前后质量守恒的原因是在化学反应前后,原子的种类、个数与质量不变。
③小明将图 C 装置改进成如图 D 所示,装置气密性良好,但是反应后天平指针向右偏转,原因是稀盐酸和石灰石在密封容器中反应且生成的二氧化碳气体没有逸出,进入气球后使气球体积膨胀,所受到的浮力变大,所以称得的质量变小。
故填:A 在化学反应前后,原子的种类、个数与质量不变 稀盐酸和石灰石在密封容器中反应且生成的二氧化碳气体没有逸出,进入气球后使气球体积膨胀,所受到的浮力变大,所以称得的质量变小

 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案