题目内容
某校化学兴趣小组同学对氯酸钾制取氧气进行了探究:测定从开始加热到收集100mL氧气所用的时间.
【实验与记录】实验一:不同催化剂对反应速率的影响
实验二:探究氯酸钾与二氧化锰的最佳比例
小组同学取1g氯酸钾与一定量的二氧化锰按一定比例混合均匀后,放入试管加热,测得数据如下表:
【分析与结论】
(1)写出“实验二”中发生反应的化学方程式 .
(2)分析实验一,氯酸钾分解的速率与 有关,在相同条件下, 的催化效果最好(填化学式)
(3)由实验二可知二氧化锰与氯酸钾的质量比为 时,反应速率最快.
(4)二氧化锰的用量过少时产生氧气的速率很慢,原因是
(5)二氧化锰的用量过多相当于减少反应物的 ,所以反应速率受到影响
(6)通过分析可知,在化学反应中催化剂的用量 越多越好.(填“是”或“不是”)
【实验与记录】实验一:不同催化剂对反应速率的影响
| 实验序号 | 1 | 2 | 3 | 4 |
| 催化剂的种类 | 二氧化锰 | 氧化铜 | 四氧化三铁 | 三氧化二铁 |
| 所用时间/s | 85 | 50 | 30 | 28 |
小组同学取1g氯酸钾与一定量的二氧化锰按一定比例混合均匀后,放入试管加热,测得数据如下表:
| 二氧化锰与氯酸钾的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 | 2:3 | 1:1 | 2:1 |
| 所用时间/s | 12.4 | 8 | 5 | 5.5 | 7.5 | 9.3 | 10.5 | 15 | 24 |
(1)写出“实验二”中发生反应的化学方程式
(2)分析实验一,氯酸钾分解的速率与
(3)由实验二可知二氧化锰与氯酸钾的质量比为
(4)二氧化锰的用量过少时产生氧气的速率很慢,原因是
(5)二氧化锰的用量过多相当于减少反应物的
(6)通过分析可知,在化学反应中催化剂的用量
考点:催化剂的特点与催化作用,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)氯酸钾与二氧化锰反应,生成氯化钾和氧气,据此写出化学反应式;
(2)根据图表中的数据分析,所用时间少的就是反应速率快的;
(3)根据图表中的数据分析,所用时间少的就是反应速率快的;
(4)根据反应速度的影响因素主要是反应物的接触面积来考虑;
(5)根据混合物的混合情况考虑,催化剂多了相对来说反应物就少了,反应速度就收到了影响;
(6)由实验现象分析结论,再通过表格上的数据能看出催化剂的用量与反应速度的关系.
(2)根据图表中的数据分析,所用时间少的就是反应速率快的;
(3)根据图表中的数据分析,所用时间少的就是反应速率快的;
(4)根据反应速度的影响因素主要是反应物的接触面积来考虑;
(5)根据混合物的混合情况考虑,催化剂多了相对来说反应物就少了,反应速度就收到了影响;
(6)由实验现象分析结论,再通过表格上的数据能看出催化剂的用量与反应速度的关系.
解答:解:(1)氯酸钾与二氧化锰反应,生成氯化钾和氧气,反应的方程式为2KClO3
2KCl+3O2↑;
故答案为:2KClO3
2KCl+3O2↑;
(2)实验一中不同种类的催化剂,反应所需时间不同,就是说氯酸钾分解的速率与催化剂有关,在相同条件下,Fe2O3的催化效果最好;
故答案为:催化剂;Fe2O3;
(3)通过观察图表中的数据可知,二氧化锰与氯酸钾的质量比是1:10时,所用的时间最少,反应速率最快.
故答案为:1:10;
(4)反应速度的影响因素主要是反应物的接触面积,接触面积越大反应速度就越快,二氧化锰的用量过少与氯酸钾的接触面积就越小,所以反应速度慢;
故答案为:MnO2与KClO3的接触面积小,因此催化作用不明显;
(5)二氧化锰用量过多氯酸钾的质量分数就降低了,反应物的接触面积就少了,就影响了反应速度;
故答案为:质量分数.
(6)通过上面的表格显示的内容可知在化学反应中催化剂的用量并不是越多越好.
故答案为:不是.
| ||
| △ |
故答案为:2KClO3
| ||
| △ |
(2)实验一中不同种类的催化剂,反应所需时间不同,就是说氯酸钾分解的速率与催化剂有关,在相同条件下,Fe2O3的催化效果最好;
故答案为:催化剂;Fe2O3;
(3)通过观察图表中的数据可知,二氧化锰与氯酸钾的质量比是1:10时,所用的时间最少,反应速率最快.
故答案为:1:10;
(4)反应速度的影响因素主要是反应物的接触面积,接触面积越大反应速度就越快,二氧化锰的用量过少与氯酸钾的接触面积就越小,所以反应速度慢;
故答案为:MnO2与KClO3的接触面积小,因此催化作用不明显;
(5)二氧化锰用量过多氯酸钾的质量分数就降低了,反应物的接触面积就少了,就影响了反应速度;
故答案为:质量分数.
(6)通过上面的表格显示的内容可知在化学反应中催化剂的用量并不是越多越好.
故答案为:不是.
点评:此题探究实验室用二氧化锰与氯酸钾制取氧气时,二氧化锰作催化剂的量要适中,过多或过少反应速率都或受到影响.希望同学们作此试验时注意二氧化锰的用量,节约药品.

练习册系列答案
相关题目
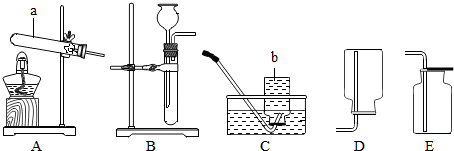
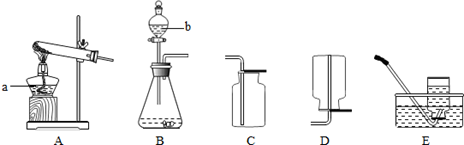

 图I是实验室“制取氢气并还原氧化铜实验”的简易装置,其中铜制燃烧匙可以在试管M中上下移动,虚线框中的装置需从图Ⅱ中选取.
图I是实验室“制取氢气并还原氧化铜实验”的简易装置,其中铜制燃烧匙可以在试管M中上下移动,虚线框中的装置需从图Ⅱ中选取.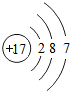 请根据下表,回答问题:
请根据下表,回答问题: