题目内容
【题目】向10g CaCO3中不断加入稀盐酸,其质量变化如图所示,请回答下列问题: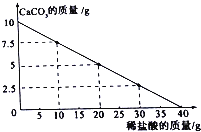
①当10gCaCO3恰好完全反应时,所加稀盐酸的质量为________ .
②所加稀盐酸的溶质质量分数为多少?(写出计算过程,结果精确到0.01%)
【答案】解:①如图象所示:当10gCaCO3恰好完全反应时,所加稀盐酸的质量40g
②解:设40g稀盐酸含有HCl的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
10g x![]()
![]() X=7.3g
X=7.3g
答:所加稀盐酸的溶质质量分数为![]()
![]() =18.25%
=18.25%
【解析】①由图象可知:当CaCO3质量为0时,即为盐酸与CaCO3恰好完全反应的时刻,此时所用稀盐酸的量即是所消耗的稀盐酸,故10g CaCO3完全反应时,所加稀盐酸的质量为40g.②根据碳酸钙与盐酸反应的化学方程式,由碳酸钙的质量可以计算出消耗的稀盐酸的溶质质量,由溶质质量分数计算公式即可求出稀盐酸的溶质质量分数.
【考点精析】本题主要考查了根据化学反应方程式的计算的相关知识点,需要掌握各物质间质量比=系数×相对分子质量之比才能正确解答此题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】下列对一些事实的解释错误的是( )
事 实 | 解 释 | |
A | 热胀冷缩 | 分子的大小随温度升降而改娈 |
B | 酒香不怕巷子深 | 分子不断的运动 |
C | CO有毒而CO2无毒 | 两种物质的分子构成不同 |
D | 电解水生成氢气和氧气 | 分子发生改变 |
A. A B. B C. C D. D