题目内容
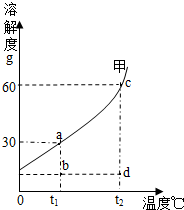 甲物质在水中的溶解度曲线如图,a、b、c、d为图象中的四个点.
甲物质在水中的溶解度曲线如图,a、b、c、d为图象中的四个点.(1)t1℃时,50g水中最多能溶解甲物质
15
15
g.(2)t2℃时,甲物质的溶解度是
60
60
g.(3)要使甲物质的饱和溶液成为不饱和溶液,可采用的一种方法是
升高温度(或加入水)
升高温度(或加入水)
.(4)甲物质的溶液分别处于a、b、c、d四点时,溶液中甲物质的溶质质量分数大小关系正确的是
Ⅲ
Ⅲ
(选填下列编号).Ⅰ、c>d=b>aⅡ、c=d>a=b
Ⅲ、c>a>b=dⅣ、c>a=b>d
(5)若要得到溶质质量分数为30%以上的甲溶液,配制时的温度应不低于
t1
t1
℃.分析:(1)根据t1℃时甲的溶解度分析解答;
(2)根据溶解度曲线可知某一温度下物质的溶解度;
(3)根据甲的溶解度曲线及饱和溶液、不饱和溶液的转化分析;
(4)根据甲的溶解度随温度变化情况及饱和溶液中溶质的质量分数计算分析解答;
(5)根据饱和时质量分数的计算式:
×100%,可知一定温度下,饱和溶液溶质的质量分数最大,并据此分析.
(2)根据溶解度曲线可知某一温度下物质的溶解度;
(3)根据甲的溶解度曲线及饱和溶液、不饱和溶液的转化分析;
(4)根据甲的溶解度随温度变化情况及饱和溶液中溶质的质量分数计算分析解答;
(5)根据饱和时质量分数的计算式:
| 溶解度 |
| 溶解度+100g |
解答:解:(1)t1℃时甲的溶解度是30g,所以50g水中最多能溶解甲物质15g;
(2)t2℃时,甲物质的溶解度是60g;
(3)甲的溶解度随温度的升高而增大,所以要使甲物质的饱和溶液成为不饱和溶液,可采用增加溶剂或升高温度的方法;
(4)由图可知甲的溶解度随温度的升高而增大,同一温度下溶解度相等,饱和溶液的溶质质量分数大于不饱和溶液;t2℃时甲的溶解度大于t1℃时甲的溶解度,饱和溶液甲从t2℃时降低温度到t1℃时,饱和溶液的溶质质量分数减小,t2℃时饱和溶液的溶质质量分数大于于t1℃时饱和溶液的溶质质量分数,故溶质质量分数由大到小的顺序是:c>a>b=d;
(5)t1℃时甲的溶解度是30g,根据饱和时质量分数的计算式:
×100%,所以要得到溶质质量分数为30%以上的甲溶液,配制时的温度应不低于t1℃;
故答案为:
(1)15;
(2)60;
(3)升高温度(或加入水);
(4)Ⅲ;
(5)t1.
(2)t2℃时,甲物质的溶解度是60g;
(3)甲的溶解度随温度的升高而增大,所以要使甲物质的饱和溶液成为不饱和溶液,可采用增加溶剂或升高温度的方法;
(4)由图可知甲的溶解度随温度的升高而增大,同一温度下溶解度相等,饱和溶液的溶质质量分数大于不饱和溶液;t2℃时甲的溶解度大于t1℃时甲的溶解度,饱和溶液甲从t2℃时降低温度到t1℃时,饱和溶液的溶质质量分数减小,t2℃时饱和溶液的溶质质量分数大于于t1℃时饱和溶液的溶质质量分数,故溶质质量分数由大到小的顺序是:c>a>b=d;
(5)t1℃时甲的溶解度是30g,根据饱和时质量分数的计算式:
| 溶解度 |
| 溶解度+100g |
故答案为:
(1)15;
(2)60;
(3)升高温度(或加入水);
(4)Ⅲ;
(5)t1.
点评:根据溶解度曲线可知某温度下物质的溶解度、溶解度随温度的变化趋势,并分析饱和溶液、不饱和溶液的相互转化方法,溶质的质量分数分析等.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
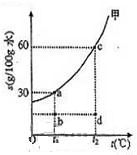 (2010?上海)甲物质在水中的溶解度曲线如图,a、b、c、d为图象中的四个点.
(2010?上海)甲物质在水中的溶解度曲线如图,a、b、c、d为图象中的四个点.
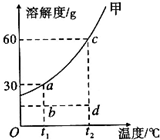 甲物质在水中的溶解度曲线如图,a、b、c、d为图象中的四个点.
甲物质在水中的溶解度曲线如图,a、b、c、d为图象中的四个点.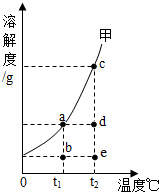 确的是( )
确的是( )