题目内容
右图为实验室研究炼铁的化学原理的装置,请回答和该实验有关的问题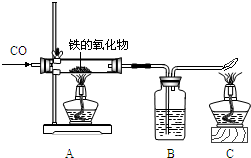
(1)A处玻璃管中发生反应的化学方程式为
(2)B处的实验现象
(3)C处酒精灯的作用
(4)现有含杂质的氧化铁样品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
| 反应前 | 氧化铁完全反应后 | |
| 甲组 | 洗气瓶和石灰水的质量为190g | 洗气瓶和石灰水的质量为196g |
| 乙组 | 玻璃管和氧化铁样品的质量为57.9g | 玻璃管和氧化铁样品的质量为55.2g |
分析:(1)玻璃管中为一氧化碳还原氧化铁,产物为铁和二氧化碳;
(2)二氧化碳能使澄清石灰水变浑浊;
(3)一氧化碳有毒,不能直接排放到空气中,需进行尾气处理;
(4)从理论上分析,玻璃管中固体减少的质量即为氧化铁中氧元素的质量,洗气瓶中石灰水增重的质量为反应产生二氧化碳的质量,利用这两个数据都可以计算出样品中氧化铁的质量分数,但是氢氧化钙为微容物,澄清石灰水浓度很小,很难将二氧化碳全部吸收,所以若用石灰水增重计算,结果可能会不准确.
(2)二氧化碳能使澄清石灰水变浑浊;
(3)一氧化碳有毒,不能直接排放到空气中,需进行尾气处理;
(4)从理论上分析,玻璃管中固体减少的质量即为氧化铁中氧元素的质量,洗气瓶中石灰水增重的质量为反应产生二氧化碳的质量,利用这两个数据都可以计算出样品中氧化铁的质量分数,但是氢氧化钙为微容物,澄清石灰水浓度很小,很难将二氧化碳全部吸收,所以若用石灰水增重计算,结果可能会不准确.
解答:解:(1)A处玻璃管中发生反应的化学方程式为3CO+Fe2O3
2Fe+3CO2;
(2)二氧化碳能使澄清石灰水变浑浊,所以B处的实验现象是变浑浊;
(3)一氧化碳有毒,将其点燃可消除污染;
(4)选择乙组数据计算更为准确,玻璃管中固体减少的质量即为氧化铁中氧元素的质量,则氧化铁为:
=9g,样品中氧化铁的质量分数为:
×100%=90%;
故答案为:(1)3CO+Fe2O3
2Fe+3CO2;
(2)变浑浊;
(3)点燃CO,消除其污染;
(4)乙、90%
| ||
(2)二氧化碳能使澄清石灰水变浑浊,所以B处的实验现象是变浑浊;
(3)一氧化碳有毒,将其点燃可消除污染;
(4)选择乙组数据计算更为准确,玻璃管中固体减少的质量即为氧化铁中氧元素的质量,则氧化铁为:
| 57.9g-55.2g |
| 30% |
| 9g |
| 10g |
故答案为:(1)3CO+Fe2O3
| ||
(2)变浑浊;
(3)点燃CO,消除其污染;
(4)乙、90%
点评:本题是一氧化碳还原氧化铁实验,(4)小题较难,学生容易出错,容易忽略氢氧化钙微容这个隐含条件.一般检验二氧化碳选用澄清石灰水,而吸收二氧化碳则选用氢氧化钠溶液,若本题将澄清石灰水换做氢氧化钠,则也可以根据溶液增重计算样品中氧化铁的质量分数.

练习册系列答案
相关题目
右图为实验室研究炼铁的化学原理的装置,请回答和该实验有关的问题

(1)A处玻璃管中发生反应的化学方程式为________
(2)B处的实验现象________
(3)C处酒精灯的作用________
(4)现有含杂质的氧化铁样品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
| 反应前 | 氧化铁完全反应后 | |
| 甲组 | 洗气瓶和石灰水的质量为190g | 洗气瓶和石灰水的质量为196g |
| 乙组 | 玻璃管和氧化铁样品的质量为57.9g | 玻璃管和氧化铁样品的质量为55.2g |
右图为实验室研究炼铁的化学原理的装置,请回答和该实验有关的问题

(1)A处玻璃管中发生反应的化学方程式为
(2)B处的实验现象
(3)C处酒精灯的作用
(4)现有含杂质的氧化铁样品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
你认为应选择 组的数据来计算样品中氧化铁的质量分数,其结果为 .

(1)A处玻璃管中发生反应的化学方程式为
(2)B处的实验现象
(3)C处酒精灯的作用
(4)现有含杂质的氧化铁样品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
| 反应前 | 氧化铁完全反应后 | |
| 甲组 | 洗气瓶和石灰水的质量为190g | 洗气瓶和石灰水的质量为196g |
| 乙组 | 玻璃管和氧化铁样品的质量为57.9g | 玻璃管和氧化铁样品的质量为55.2g |
右图为实验室研究炼铁的化学原理的装置,请回答和该实验有关的问题

(1)A处玻璃管中发生反应的化学方程式为
(2)B处的实验现象
(3)C处酒精灯的作用
(4)现有含杂质的氧化铁样品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
你认为应选择 组的数据来计算样品中氧化铁的质量分数,其结果为 .

(1)A处玻璃管中发生反应的化学方程式为
(2)B处的实验现象
(3)C处酒精灯的作用
(4)现有含杂质的氧化铁样品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
| 反应前 | 氧化铁完全反应后 | |
| 甲组 | 洗气瓶和石灰水的质量为190g | 洗气瓶和石灰水的质量为196g |
| 乙组 | 玻璃管和氧化铁样品的质量为57.9g | 玻璃管和氧化铁样品的质量为55.2g |
右图为实验室研究炼铁的化学原理的装置,请回答和该实验有关的问题

(1)A处玻璃管中发生反应的化学方程式为
(2)B处的实验现象
(3)C处酒精灯的作用
(4)现有含杂质的氧化铁样品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
你认为应选择 组的数据来计算样品中氧化铁的质量分数,其结果为 .

(1)A处玻璃管中发生反应的化学方程式为
(2)B处的实验现象
(3)C处酒精灯的作用
(4)现有含杂质的氧化铁样品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:
| 反应前 | 氧化铁完全反应后 | |
| 甲组 | 洗气瓶和石灰水的质量为190g | 洗气瓶和石灰水的质量为196g |
| 乙组 | 玻璃管和氧化铁样品的质量为57.9g | 玻璃管和氧化铁样品的质量为55.2g |