题目内容
【题目】实验室部分仪器或装置如图所示,请回答下列问题:
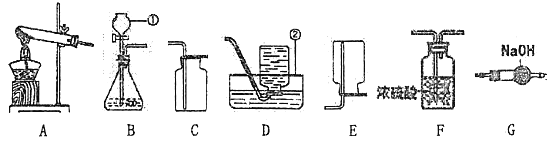
(一)气体制取:
(1)写出图中标号仪器的名称:①______ ②______
(2)写出在实验室中制取CO2气体的化学方程式______,应选择的制取装置为______,若要求收集到干燥的CO2气体,还应该增加的装置为______。(填置序号)
(3)用锌粒与稀硫酸反应制取H2,可以选用与制CO2相同的发生装置,可见制取气体时选择发生装置应考虑的因素为______和______。
(二)验证二氧化碳的性质
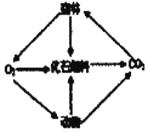
利用下图装置,验证CO2的性质。回答下列问题:
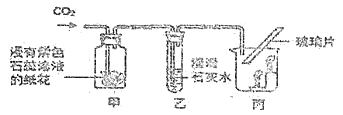
(4)甲中使石蕊变红的物质是______。(填化学式)
(5)乙中反应的化学方程式是______。
(6)丙中蜡烛由下而上依次熄灭,此现象证明二氧化碳具有______的物理性质。
【答案】分液漏斗 水槽 CaCO3+2HCl=CaCl2+H2O+CO2↑ BC F 反应物的状态 反应条件 碳酸(或H2CO3) CO2+Ca(OH)2= CaCO3↓+H2O 密度比空气大
【解析】
(1)仪器①是分液漏斗,故填分液漏斗;仪器②是水槽,故填水槽;
(2)实验室用大理石和稀盐酸反应,生成氯化钙、水和二氧化碳,方程式故填CaCO3+2HCl=CaCl2+H2O+CO2↑;反应物为固体和液体,反应不需要加热,发生装置选B,二氧化碳可溶于水且密度比空气大,收集装置选C,制取装置故填BC;若要求收集到干燥的CO2气体,用浓硫酸进行干燥,故填F;
(3)用锌粒与稀硫酸反应制取H2,可以选用与制CO2相同的发生装置,可见制取气体时选择发生装置应考虑的因素是反应物的状态和反应条件,故填反应物的状态;故填反应条件;
(4)甲中使石蕊变红的物质是二氧化碳和水反应生成的碳酸,故填碳酸(或H2CO3);
(5)澄清石灰水的二氧化碳反应生成碳酸钙沉淀和水,故填CO2+Ca(OH)2= CaCO3↓+H2O;
(6)丙中蜡烛由下而上依次熄灭,证明二氧化碳不可燃不助燃且密度比空气大的性质,属于物理性质的故填密度比空气大。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
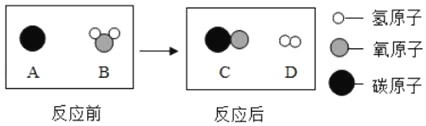
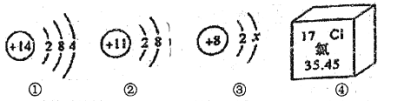
小学生10分钟应用题系列答案【题目】两他同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶先去标签的黑色粉末B。
(提出问题)这两瓶黑色粉末A和B分别是什么物质?
(猜想)甲同学:A是铁粉,B是二氧化锰。
乙同学:A是炭粉,B是氧化铜。
(查阅资料)炭粉和二氧化锰均不能与稀硫酸反应;![]()
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
①取少量A粉末于试管中,加入适量稀硫酸。 | 黑色粉末不溶解。没有气体产生。 | A粉末一定不是______。 |
②取少量B粉末于试管中,如入适量稀硫酸。 | ______。 | B粉末是氧化铜。 |
(反思与拓展)
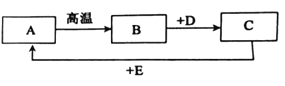
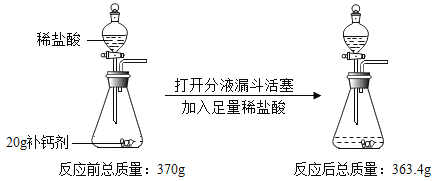
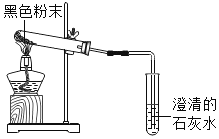
(1)将这两种黑色粉末混合加热(如图),观察到黑色粉末逐渐变为红色.澄清石灰水变浑浊,黑色粉末A和B发生反应的化学方程式为______。实验结束时,先将导管移出.再熄灭酒精灯的原因是______
(2)乙同学的猜想是正确。
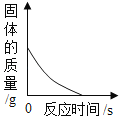
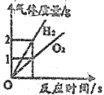
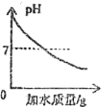
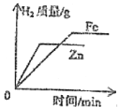
【题目】下列图象不能正确反映其变化过程的是( )
|
|
|
|
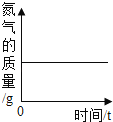
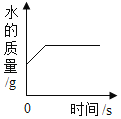
A.红磷在装有空气的密闭容器中燃烧 | B.将水通电电解一段时间 | C.向一定质量的过 氧化氢的水溶液中 加入二氧化锰 | D.向一定质量的氧 化铁中通入一氧化 碳气体并持续高温 |
A. A B. B C. C D. D