题目内容
人的胃液中含有少量 (填名称),可以帮助消化,但胃酸过多时常服含氢氧化铝的药物,其反应原理是 (原理都是用化学方程式表示).Ba2+有毒,用X射线检查肠胃病时,常服用钡餐(BaSO4 ),但误服BaCO3 可引起中毒,其反应原理是 ,中毒后,可立即服用泻盐(MgSO4)来解毒,其反应原理是 .
考点:酸的化学性质,酸的物理性质及用途,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:氢氧化铝与胃液中的盐酸发生中和反应生成氯化铝和水,能中和过量的胃酸;BaCO3能与胃液中的盐酸反应生成易溶于水的氯化钡、水和二氧化碳,生成的氯化钡易溶于水,会使人中毒;硫酸镁可以与BaCl2反应生成难溶于胃酸的BaSO4和无毒的氯化镁;据此进行分析解答.
解答:解:氢氧化铝与胃液中的盐酸发生中和反应生成氯化铝和水,能中和过量的胃酸,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O.
BaCO3能与胃液中的盐酸反应生成易溶于水的氯化钡、水和二氧化碳,生成的氯化钡易溶于水,会使人中毒,反应的化学方程式为:BaCO3+2HCl═BaCl2+H2O+CO2↑.
中毒后可立即服用泻盐(硫酸镁)来解,是因为硫酸镁可以与BaCl2反应生成难溶于胃酸的BaSO4和无毒的氯化镁,反应的化学方程式为:BaCl2+MgSO4═BaSO4↓+MgCl2.
故答案为:盐酸;Al(OH)3+3HCl═AlCl3+3H2O;BaCO3+2HCl═BaCl2+H2O+CO2↑;BaCl2+MgSO4═BaSO4↓+MgCl2.
BaCO3能与胃液中的盐酸反应生成易溶于水的氯化钡、水和二氧化碳,生成的氯化钡易溶于水,会使人中毒,反应的化学方程式为:BaCO3+2HCl═BaCl2+H2O+CO2↑.
中毒后可立即服用泻盐(硫酸镁)来解,是因为硫酸镁可以与BaCl2反应生成难溶于胃酸的BaSO4和无毒的氯化镁,反应的化学方程式为:BaCl2+MgSO4═BaSO4↓+MgCl2.
故答案为:盐酸;Al(OH)3+3HCl═AlCl3+3H2O;BaCO3+2HCl═BaCl2+H2O+CO2↑;BaCl2+MgSO4═BaSO4↓+MgCl2.
点评:本题难度不大,掌握中和反应应用、盐的化学性质、化学方程式的书写等是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在某同学的学习笔记中,对下列符号中“2”的含义有如下记载.其中正确的是( )
| A、符号2SO3中的“2”,表示2个三氧化硫分子 | ||
| B、符号O2-中的“2”,表示氧元素的化合价为-2价 | ||
| C、符号CO2中的“2”,表示一个氧分子中含有2个氧原子 | ||
D、符号
|
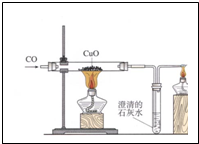 某兴趣小组利用如图装置进行试验,请回答相关的问题:
某兴趣小组利用如图装置进行试验,请回答相关的问题: 如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法正确的是
如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法正确的是