题目内容
15.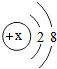 某粒子的结构示意图如图所示,若该粒子是电中性的粒子,则x=10,粒子符号为Ne,若该粒子带一个单位正电荷,则x=11,粒子符号为Na+,若该粒子带两个单位负电荷,则x=8,粒子符号为O2-.
某粒子的结构示意图如图所示,若该粒子是电中性的粒子,则x=10,粒子符号为Ne,若该粒子带一个单位正电荷,则x=11,粒子符号为Na+,若该粒子带两个单位负电荷,则x=8,粒子符号为O2-.
分析 根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
解答 解:若该粒子为中性原子,核内的质子数等于核外的电子数,所以x=2+8=10;粒子符号为Ne;
若该粒子带1个单位正电荷,为阳离子,核内的质子数是2+8+1=11,该离子是钠离子,符号是Na+;
若该粒子带2个单位负电荷,为阴离子,则x=10-2=8,该离子是氧离子,符号是O2-.
故答案为:(1)10;Ne;(2)11;Na+;(3)8;O2-.
点评 本题考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
相关题目
17.除去下列物质中所含杂质(括号内为杂质),所选用试剂及操作方法均正确的一组是( )
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaOH(Na2CO3) | 稀盐酸 | 蒸发、结晶 |
| B | CO2(CO) | 氧化铜 | 加热 |
| C | Cu(CuO) | 氧气 | 加热 |
| D | CuSO4(H2SO4) | 氢氧化钠溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
3.欲一次配制100g5%的氢氧化钠溶液需要用到的一组仪器是( )
| A. | 100mL量筒、天平、玻璃棒 | |
| B. | 100mL量筒、50mL烧杯、天平、玻璃棒 | |
| C. | 100mL量筒、酒精灯、天平、玻璃棒 | |
| D. | 100mL量筒、200mL烧杯、天平、玻璃棒 |