题目内容
【题目】某校化学兴趣小组同学用一瓶含有杂质氯化钠的硫酸钠固体样品,进行如图所示的实验.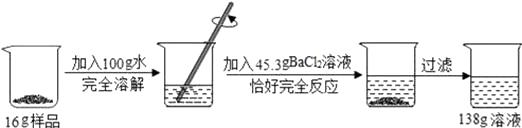
请根据以上信息计算:
(1)该实验中生成沉淀的质量。
(2)反应后所的溶液中溶质的质量分数(精确到0.1%)。
【答案】
(1)解: 该实验中生成沉淀的质量∶16g+100g+45.3g-138g=23.3g.
答∶该实验中生成沉淀的质量是23.3g.
(2)解∶设反应后生成氯化钠质量为x,样品中硫酸钠质量为y
Na2SO4 +BaCl2 = | Ba SO4↓+ | 2NaCl |
142 | 233 | 117 |
y | 23.3g | x |
![]() =
= ![]() ,x=11.7g,
,x=11.7g, ![]() =
= ![]() ,y=14.2g.
,y=14.2g.
反应后所的溶液中溶质的质量分数∶ ![]() ×100%=9.8%.
×100%=9.8%.
答∶反应后所的溶液中溶质的质量分数是9.8%.
【解析】(1)该实验中生成沉淀的质量∶16g+100g+45.3g-138g=23.3g
(2)设反应后生成氯化钠质量为x,样品中硫酸钠质量为y
Na2SO4 +BaCl2 = | Ba SO4↓+ | 2NaCl |
142 | 233 | 117 |
y | 23.3g | x |
![]() =
= ![]() ,x=11.7g,
,x=11.7g, ![]() =
= ![]() ,y=14.2g.
,y=14.2g.
反应后所的溶液中溶质的质量分数∶ ![]() ×100%=9.8%.
×100%=9.8%.
答∶反应后所的溶液中溶质的质量分数是9.8%.
利用差量法计算出生成的沉淀质量,在利用沉淀质量在化学方程式中计算出参加反应的硫酸钠的质量,反应生成的氯化钠的质量,在利用溶质的质量分数计算公式![]() 计算出氯化钠溶液中溶质的质量分数。
计算出氯化钠溶液中溶质的质量分数。
在进行化学方程式与溶液计算相结合的综合计算时,要注意以下问题:1.在根据化学方程式列有关反应物、生成物的质量比时,要以溶质的质量列比例,而不能用溶液质量或体积列比例。2.反应后所得溶液质量用质量守恒法:溶液质量=反应物的质量总和—化学方程式中带箭头的物质的质量(沉淀或气体)—反应物中不参与化学反应的固体杂质的质量。3.反应物中的不溶性杂质或剩余物不能算入反应物质量总和,也不能算入反应后剩余溶液的质量。4.溶质质量:反应后溶液中溶质的质量可能会有两个来源,反应生成的和原混合物中的,计算时不能有遗漏,即反应后溶液中溶质质量=生成的溶质质量+原混合物中存在的溶质质量。