题目内容
金属材料是现代生活和工业生产中应用极为普遍的一类物质.
(1)钛合金是21世纪的重要材料,具有熔点高、可塑性好、抗腐蚀性强、与人体有很好的“相容性”等优良性能.金属的下列用途:①用来做保险丝 ②用来制人造骨 ③用于制造船舶.其中与钛合金性质不符合的是______(填序号).
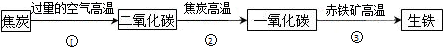
(2)铁是一种最主要的金属材料,实验室里用一氧化碳还原氧化铁得到铁,实验过程中,先通入一氧化碳目的是______.炼铁厂常以焦炭、赤铁矿、空气等为主要原料炼铁,反应过程如下:

写出②③两步的化学方程式______、______.
(3)矿物的储量有限,而且不可再生,我们必须保护金属资源并进行金属的回收利用.
某兴趣小组同学欲从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部金属铜,应先加入过量的______,反应的化学方程式为:______、______.充分反应后过滤,滤渣中含有______.继续处理,加入适量______可以得到纯净的金属铜和硫酸亚铁.
解:(1)钛合金具有熔点高的性质,因此不能用来做保险丝;可塑性好、抗腐蚀性强、与人体有很好的“相容性”等优良性能,因此用来制人造骨、用于制造船舶等;故答案为:①
(2)实验室里用一氧化碳还原氧化铁得到铁,实验过程中,先通入一氧化碳目的是排净空气,防止爆炸;在炼铁的过程中,发生的化学反应有:①碳和氧气在点燃的条件下生成二氧化碳;②二氧化碳和碳在高温的条件下生成一氧化碳;③一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;故答案为:排净空气,防止爆炸; CO2+C 2CO;3CO+Fe2O3
2CO;3CO+Fe2O3  2Fe+3CO2
2Fe+3CO2
(3)从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部金属铜,应先加入过量的铁粉,铁与硫酸反应生成硫酸亚铁和氢气,铁与硫酸铜溶液反应生成硫酸亚铁和铜;充分反应后过滤,滤渣中含有生成的铜和过量的铁;在铁和铜的混合物中加入适量的稀硫酸,可以得到纯净的金属铜,故答案为:Fe; Fe+H2SO4=FeSO4+H2↑;Fe+CuSO4=FeSO4+Cu; Fe、Cu; 稀硫酸
分析:钛合金具有熔点高的性质,因此不能用来做保险丝;可塑性好、抗腐蚀性强、与人体有很好的“相容性”等优良性能,因此用来制人造骨、用于制造船舶等;实验室里用一氧化碳还原氧化铁得到铁,实验过程中,先通入一氧化碳目的是排净空气,防止爆炸;在炼铁的过程中,发生的化学反应有:①碳和氧气在点燃的条件下生成二氧化碳;②二氧化碳和碳在高温的条件下生成一氧化碳;③一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可.从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部金属铜,应先加入过量的铁粉,铁与硫酸反应生成硫酸亚铁和氢气,铁与硫酸铜溶液反应生成硫酸亚铁和铜;充分反应后过滤,滤渣中含有生成的铜和过量的铁;在铁和铜的混合物中加入适量的稀硫酸,可以得到纯净的金属铜.
点评:本题既考查了合金与合金的性质、炼铁的原理,又考查了金属的性质和化学方程式的书写等,要理解合金的性质,即合金的硬度大,熔点低,耐腐蚀.本考点综合性强,要好好把握.
(2)实验室里用一氧化碳还原氧化铁得到铁,实验过程中,先通入一氧化碳目的是排净空气,防止爆炸;在炼铁的过程中,发生的化学反应有:①碳和氧气在点燃的条件下生成二氧化碳;②二氧化碳和碳在高温的条件下生成一氧化碳;③一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;故答案为:排净空气,防止爆炸; CO2+C
 2CO;3CO+Fe2O3
2CO;3CO+Fe2O3  2Fe+3CO2
2Fe+3CO2(3)从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部金属铜,应先加入过量的铁粉,铁与硫酸反应生成硫酸亚铁和氢气,铁与硫酸铜溶液反应生成硫酸亚铁和铜;充分反应后过滤,滤渣中含有生成的铜和过量的铁;在铁和铜的混合物中加入适量的稀硫酸,可以得到纯净的金属铜,故答案为:Fe; Fe+H2SO4=FeSO4+H2↑;Fe+CuSO4=FeSO4+Cu; Fe、Cu; 稀硫酸
分析:钛合金具有熔点高的性质,因此不能用来做保险丝;可塑性好、抗腐蚀性强、与人体有很好的“相容性”等优良性能,因此用来制人造骨、用于制造船舶等;实验室里用一氧化碳还原氧化铁得到铁,实验过程中,先通入一氧化碳目的是排净空气,防止爆炸;在炼铁的过程中,发生的化学反应有:①碳和氧气在点燃的条件下生成二氧化碳;②二氧化碳和碳在高温的条件下生成一氧化碳;③一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可.从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部金属铜,应先加入过量的铁粉,铁与硫酸反应生成硫酸亚铁和氢气,铁与硫酸铜溶液反应生成硫酸亚铁和铜;充分反应后过滤,滤渣中含有生成的铜和过量的铁;在铁和铜的混合物中加入适量的稀硫酸,可以得到纯净的金属铜.
点评:本题既考查了合金与合金的性质、炼铁的原理,又考查了金属的性质和化学方程式的书写等,要理解合金的性质,即合金的硬度大,熔点低,耐腐蚀.本考点综合性强,要好好把握.

练习册系列答案
相关题目
 金属材料是现代生活和工业生产中应用极为普遍的一类物质.
金属材料是现代生活和工业生产中应用极为普遍的一类物质.