题目内容
【题目】金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)下图是铝的原子结构示意图。下列说法不正确的是___。
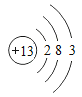
A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
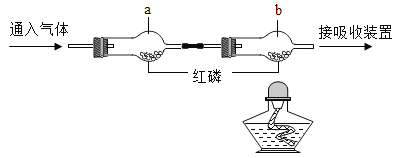
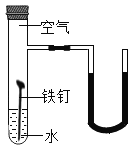
(2)下边是某探究实验装置图。一段时间后,能观察到什么现象?(装置气密性良好,且开始时U型管两端的红墨水液面相平)___
(3)X、Y、Z是三种金属固体,将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化;将X和Z浸入硝酸银溶液中,X表面有银析出而Z无变化。
①判断X、Y、Z和银四种金属的活动性由强到弱的顺序。____
②依据常见金属的活动性顺序具体确定X后,写出X与硝酸银溶液反应的化学方程式。___
(4)若将一定质量的Al放入Cu(NO3)2和Mg(NO3)2的混合溶液中,充分反应后过滤,所得滤液一定含有的溶质是____。
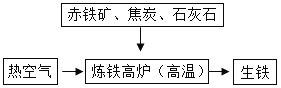
(5)下图是工业炼铁示意图。其中,焦炭的作用是燃烧提供能量和____;有铁生成的化学方程式为____。
(6)65g锌恰好与500g某硫酸完全起反应。试计算这种硫酸中溶质的质量分数_____。
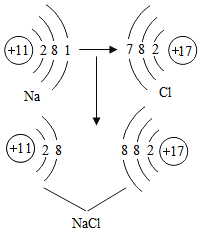
【答案】C 铁钉生锈且U型管内的液面左高右低 Y>X>Ag>Z Cu+2AgNO3=Cu(NO3)2+2Ag Al(NO3)2、Mg(NO3)2 制取CO 3CO+Fe2O3![]() 2Fe+3CO2 19.6%
2Fe+3CO2 19.6%
【解析】
(1)A.由图可知,铝原子的质子数为13,正确,不符合题意;
B.铝原子结构示意图中,最外层的电子数是3,一失去3个电子,故在化合物中铝通常显+3价,正确,不符合题意;
C.地壳中含量最多的元素氧元素,故错误,符合题意;
D.铝可作导线是由于它具有良好的导电性,正确,不符合题意。故选C。
(2)铁钉与水和空气中的氧气接触反应,消耗了管中的氧气,故内压降低, U型管内的液面左高右低。故填:铁钉生锈且U型管内的液面左高右低。
(3)①将X和Y浸入稀硫酸中,Y溶解并产生氢气,X无变化,说明Y比X活泼;将X和Z浸入硝酸银溶液中,X表面有银析出而Z无变化,说明X比银活泼,银比Z活泼,故顺序为:Y>X>Ag>Z。
②由题干可知,X在H的后面,银的前面,常见的金属是铜,铜与硝酸银反应生成银和硝酸铜,反应的方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag
(4)铝、铜、镁的金属活动性顺序为:Mg>Al>Cu,故若将一定质量的Al放入Cu(NO3)2和Mg(NO3)2的混合溶液中,铝与Cu(NO3)2反应,不和Mg(NO3)2反应,故充分反应后过滤滤液中一定有生成的硝酸铝和没有反应的硝酸镁。
(5)工业炼铁中,焦炭的作用是燃烧提供能量和制取还原剂一氧化碳。
(6)设H2SO4的质量为x
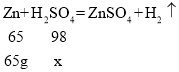
![]()
解得:x=98g
这种硫酸中溶质的质量分数为:![]() ×100%=19.6%
×100%=19.6%
答:这种硫酸中溶质的质量分数为19.6%

 阅读快车系列答案
阅读快车系列答案【题目】“黄铜”是铜和锌的合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下。(烧杯质量均为56.5克)
1 | 甲 | 乙 | 丙 |
烧杯+稀盐酸质量 | 98.0g | 93.0g | 93.0g |
加入黄铜样品质量 | 10.0g | 12.0g | 10.0g |
充分反应后,烧杯+剩余物质质量 | 107.9g | 104.9g | 102.9g |
请回答下列问题:
(1)_____同学用的稀盐酸和黄铜样品恰好完全反应,他制取的氢气的质量是_____。
(2)计算黄铜样品中锌的质量分数_____(要求写出计算过程)。
(3)计算盐酸的质量分数为_____。