题目内容
我校化学兴趣小组的同学想探究:我市盱眙县石灰石厂开采出的石灰石样品中碳酸钙的含量.他们称取12.5g该样品放入烧杯中,向其中加入了105.4g稀盐酸,恰好完全反应后(样品中的杂质不与盐酸反应,也不溶于水,不考虑CO2的溶解),共收集到二氧化碳气体4.4g.求:
(1)求样品中碳酸钙的质量分数是多少?
(2)恰好完全反应后,所得溶液中溶质质量分数是多少?
解:(1)设碳酸钙的质量为x,生成的氯化钙的质量为y.
则CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
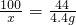
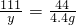
解得x=10g,y=11.1g,
该样品中碳酸钙的质量分数为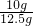 ×100%=80%
×100%=80%
答:样品中碳酸钙的质量分数是80%;
(3)因杂质既不溶于水,也不与其他物质反应,
则溶液的质量为12.5g+105.4g-(12.5g-10g)-4.4g=111g
溶质的质量为11.1g
则溶质的质量分数为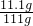 ×100%=10%,
×100%=10%,
答:反应后所得溶液中溶质的质量分数为10%.
故答案为:(1)80%;(2)10%.
分析:(1)将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量,再计算碳酸钙的质量分数;
(2)利用化学反应方程式计算出氯化钙的质量,再利用溶液的质量来计算溶质的质量分数.
点评:本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.
则CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
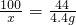
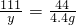
解得x=10g,y=11.1g,
该样品中碳酸钙的质量分数为
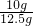 ×100%=80%
×100%=80%答:样品中碳酸钙的质量分数是80%;
(3)因杂质既不溶于水,也不与其他物质反应,
则溶液的质量为12.5g+105.4g-(12.5g-10g)-4.4g=111g
溶质的质量为11.1g
则溶质的质量分数为
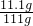 ×100%=10%,
×100%=10%,答:反应后所得溶液中溶质的质量分数为10%.
故答案为:(1)80%;(2)10%.
分析:(1)将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量,再计算碳酸钙的质量分数;
(2)利用化学反应方程式计算出氯化钙的质量,再利用溶液的质量来计算溶质的质量分数.
点评:本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目