题目内容
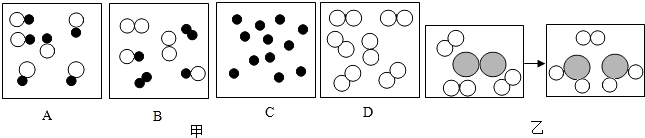
【题目】某同学设计了如图气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色.请看图回答问题: 
(1)A中反应的化学方程式;B中白磷不燃烧,原因是 .
(2)C、D中看到的现象分别是、 .
(3)用化学方程式表示E中颜色变化的原因;用F装置收集气体的依据是 .
【答案】
(1)2H2O2 ![]() 2H2O+O2↑;温度没有达到白磷的着火点
2H2O+O2↑;温度没有达到白磷的着火点
(2)C中液面下降;稀盐酸进入D中,产生大量气泡
(3)CO2+H2O=H2CO3;二氧化碳密度比空气大
【解析】解:(1)过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,反应的方程式为:2H2O2 ![]() 2H2O+O2↑;白磷与氧气接触时没有燃烧,说明温度没有达到白磷的着火点;故填:2H2O2
2H2O+O2↑;白磷与氧气接触时没有燃烧,说明温度没有达到白磷的着火点;故填:2H2O2 ![]() 2H2O+O2↑;温度没有达到白磷的着火点;(2)C装置中,氧气不断增多,压强增大,把稀盐酸压入D中,能够观察到C中液面下降,稀盐酸与石灰石接触后,反应生成氯化钙、水和二氧化碳,能够观察到D中稀盐酸进入,有大量气泡产生;故填:C中液面下降;稀盐酸进入D中,产生大量气泡;(3)E中导管口有气泡冒出,说明二氧化碳进入石蕊试液中,二氧化碳能和石蕊试液中的水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色,因此溶液由紫色变为红色;因为氧气的密度比空气的大,所以利用向上排空气法收集.
2H2O+O2↑;温度没有达到白磷的着火点;(2)C装置中,氧气不断增多,压强增大,把稀盐酸压入D中,能够观察到C中液面下降,稀盐酸与石灰石接触后,反应生成氯化钙、水和二氧化碳,能够观察到D中稀盐酸进入,有大量气泡产生;故填:C中液面下降;稀盐酸进入D中,产生大量气泡;(3)E中导管口有气泡冒出,说明二氧化碳进入石蕊试液中,二氧化碳能和石蕊试液中的水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色,因此溶液由紫色变为红色;因为氧气的密度比空气的大,所以利用向上排空气法收集.
故填:CO2+H2O=H2CO3;二氧化碳密度比空气大.
【考点精析】本题主要考查了二氧化碳的化学性质和书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应;注意:a、配平 b、条件 c、箭号才能正确解答此题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目