题目内容
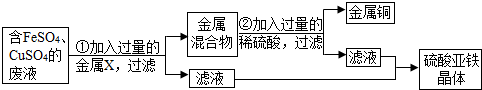
(2013?桂林)化学兴趣小组的同学们探究用Fe从含Fe2(SO4)3和CuSO4的溶液中获取金属Cu的原理.请你一起参与探究.
(1)实验依据:金属活动顺序.请在下表对应的方框内填入铁和铜的元素符号.

(2)意外发现:小明将光亮的铁丝插入含Fe2(SO4)3和CuSO4的废液中,一段时间后取出,意外地发现铁丝表面没有变红.
(3)提出问题:Fe为什么没有从废液中置换出Cu?
(4)提出假设:小丽认为在铁丝表面可能有Cu析出,但被Fe2(SO4)3溶液溶解了.
(5)验证假设:提供的主要实验用品:洁净的铁丝和铜丝各两根,相同体积、相同浓度的Fe2(SO4)3溶液三份[Fe2(SO4)3溶液显黄色].
(6)实验结论:小丽的假设
(7)思考与交流:
①兴趣小组的同学们通过对上述实验的分析,找到了用Fe从含Fe2(SO4)3和CuSO4的溶液中提取金属Cu的关键,并且最终实验获得了成功,其实验成功的关键是:
②已知Fe和Fe2(SO4)3发生化合反应.请按反应顺序写出用Fe从含Fe2(SO4)3和CuSO4的溶液中获取金属Cu的化学方程式:
(1)实验依据:金属活动顺序.请在下表对应的方框内填入铁和铜的元素符号.

(2)意外发现:小明将光亮的铁丝插入含Fe2(SO4)3和CuSO4的废液中,一段时间后取出,意外地发现铁丝表面没有变红.
(3)提出问题:Fe为什么没有从废液中置换出Cu?
(4)提出假设:小丽认为在铁丝表面可能有Cu析出,但被Fe2(SO4)3溶液溶解了.
(5)验证假设:提供的主要实验用品:洁净的铁丝和铜丝各两根,相同体积、相同浓度的Fe2(SO4)3溶液三份[Fe2(SO4)3溶液显黄色].
| 实验操作 | 实验现象和数据 | 结论 |
| ①准确称量洁净的铁丝和铜丝的质量 | 铁丝质量为ag, 铜丝质量为bg |
\ |
| ②将铁丝插入Fe2(SO4)3溶液中,一段时间后取出、洗净、干燥、称量 | 铁丝质量为mg,(m<a),溶液有黄色变为浅绿色 | 一定有 FeSO4 FeSO4 生成(填化学式) |
| ③将铜丝插入Fe2(SO4)3溶液中,一段时间后取出、洗净、干燥、称量 | 铜丝质量为ng(n<b) | 铜 能 能 (填“能”或“不能”)与Fe2(SO4)3溶液反应 |
| ④另取相同质量、相同粗细的洁净铁丝和铜丝互相缠绕,插入Fe2(SO4)3溶液中,一段时间后取出、洗净、干燥、分别称量铁丝和铜丝的质量 | 铁丝质量较轻 铜丝质量不变 |
Fe、Cu共存时 Fe Fe 优先与Fe2(SO4)3溶液反应 |
不成立
不成立
(选填“成立”或“不成立”),理由是Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应
Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应
;(7)思考与交流:
①兴趣小组的同学们通过对上述实验的分析,找到了用Fe从含Fe2(SO4)3和CuSO4的溶液中提取金属Cu的关键,并且最终实验获得了成功,其实验成功的关键是:
加入过量的铁
加入过量的铁
.并且反应充分.②已知Fe和Fe2(SO4)3发生化合反应.请按反应顺序写出用Fe从含Fe2(SO4)3和CuSO4的溶液中获取金属Cu的化学方程式:
Fe+Fe2(SO4)3=3FeSO4
Fe+Fe2(SO4)3=3FeSO4
;Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
.分析:(1)熟记金属活动性顺序表,铁排在氢的前面,铜排在氢的后面;
(5)②溶液由黄色变为浅绿色,是解题的突破口,得知溶液为硫酸亚铁溶液;
③根据实验现象中固体质量的减少,判断反应是否发生了;
④根据实验后的现象“铁丝质量较轻,铜丝质量不变”进行判断;
(6)实验结论“Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应”可以反驳小丽的假设;
(7)①铁先于硫酸铁溶液反应生成硫酸亚铁,再与硫酸铜溶液反应生成铜和硫酸亚铁溶液;
②已知Fe和Fe2(SO4)3发生化合反应,且生成的浅绿色溶液;铁与硫酸铜溶液的反应属于置换反应是教材上学过的反应方程式.
(5)②溶液由黄色变为浅绿色,是解题的突破口,得知溶液为硫酸亚铁溶液;
③根据实验现象中固体质量的减少,判断反应是否发生了;
④根据实验后的现象“铁丝质量较轻,铜丝质量不变”进行判断;
(6)实验结论“Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应”可以反驳小丽的假设;
(7)①铁先于硫酸铁溶液反应生成硫酸亚铁,再与硫酸铜溶液反应生成铜和硫酸亚铁溶液;
②已知Fe和Fe2(SO4)3发生化合反应,且生成的浅绿色溶液;铁与硫酸铜溶液的反应属于置换反应是教材上学过的反应方程式.
解答:解:(1)熟记金属活动性顺序表,并会写元素符号,故答案为:Fe Cu;
(5)②根据反应后铁丝的质量减少了,并且溶液由黄色变为浅绿色,确定为硫酸亚铁溶液,故答案为:FeSO4
③将铜丝插入Fe2(SO4)3溶液中,一段时间后取出、洗净、干燥、称量,铜丝质量为ng(n<b),铜能与Fe2(SO4)3溶液反应,故答案为:能;
④根据实验后的现象“铁丝质量较轻,铜丝质量不变”得知Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应,故答案为:Fe;
(6)用Fe从含Fe2(SO4)3和CuSO4的溶液中获取金属Cu,实验过程Fe没有从废液中置换出Cu,小丽认为在铁丝表面可能有Cu析出,但被Fe2(SO4)3溶液溶解了.但是根据实验探究的结果发现Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应,所以小丽的假设错误的,故答案为:不成立;Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应;
(7)①根据实验探究的结果,我们得知铁先于硫酸铁溶液反应生成硫酸亚铁,所以只有加入过量的铁才能发生铁与硫酸铜溶液的置换反应,从而生成铜,故答案为:加入过量的铁;
②已知Fe和Fe2(SO4)3发生化合反应,且生成的是浅绿色的溶液;铁与硫酸铜溶液的反应属于置换反应是教材上学过的反应方程式,故答案为:
Fe+Fe2(SO4)3=3FeSO4 Fe+CuSO4=FeSO4+Cu
(5)②根据反应后铁丝的质量减少了,并且溶液由黄色变为浅绿色,确定为硫酸亚铁溶液,故答案为:FeSO4
③将铜丝插入Fe2(SO4)3溶液中,一段时间后取出、洗净、干燥、称量,铜丝质量为ng(n<b),铜能与Fe2(SO4)3溶液反应,故答案为:能;
④根据实验后的现象“铁丝质量较轻,铜丝质量不变”得知Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应,故答案为:Fe;
(6)用Fe从含Fe2(SO4)3和CuSO4的溶液中获取金属Cu,实验过程Fe没有从废液中置换出Cu,小丽认为在铁丝表面可能有Cu析出,但被Fe2(SO4)3溶液溶解了.但是根据实验探究的结果发现Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应,所以小丽的假设错误的,故答案为:不成立;Fe、Cu共存时Fe优先与Fe2(SO4)3溶液反应;
(7)①根据实验探究的结果,我们得知铁先于硫酸铁溶液反应生成硫酸亚铁,所以只有加入过量的铁才能发生铁与硫酸铜溶液的置换反应,从而生成铜,故答案为:加入过量的铁;
②已知Fe和Fe2(SO4)3发生化合反应,且生成的是浅绿色的溶液;铁与硫酸铜溶液的反应属于置换反应是教材上学过的反应方程式,故答案为:
Fe+Fe2(SO4)3=3FeSO4 Fe+CuSO4=FeSO4+Cu
点评:本题联系生产实际以实验探究的形式,重在考查金属的化学性质,虽难度稍大,但仍是一道不错的化学题.

练习册系列答案
相关题目