题目内容
【题目】化学兴趣小组的同学欲回收三项测试化学实验操作考试(考题:鉴别碳酸钠和氯化钠两瓶白色固体)用剩的药品。他们对其中的一瓶药品是否纯净产生质疑,对其成分展开了如下探究:
(猜想与假设)猜想一:白色固体为碳酸钠;
猜想二:白色固体为氯化钠;
猜想三:白色固体为碳酸钠和氯化钠的混合物。
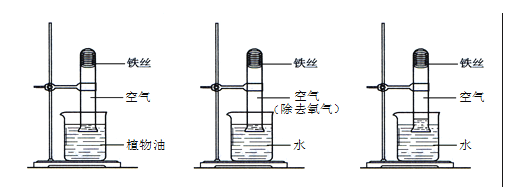
(设计与实验)取少最固体药品,装入试管,加蒸馏水溶解,进行如图实验: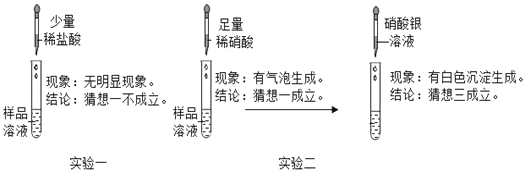
(讨论与交流)
(1)实验一①____(填“能”或“不能”)得出正确结论,你的理由是②___。
(2)实验二中向样品溶液滴加足量稀硝酸后③___(填“能”或“不能”)得出正确结论,你的理由是④______。
(3)加入稀硝酸并且至过量的目的是⑤____________。
同学们经过仔细讨论,最终确定猜想三成立。
(归纳与总结)同学们根据实验结论领悟到:在选加试剂检验物质成分时;既要考虑⑥______,又要防止⑦______。
【答案】不能碳酸钠水溶液中含有氢氧化钠,氢氧化钠先跟少量的稀盐酸反应,稀盐酸被耗尽,碳酸钠没有与稀盐酸反应,无法鉴别碳酸钠的有无不能碳酸钠与稀硝酸反应,氯化钠与稀硝酸不反应,加入稀硝酸有气泡产生只能验证碳酸钠存在,无法判断氯化钠是否存在除去氢氧化钠和碳酸钠,并验证碳酸钠是否存在除尽原有的干扰物质引入新的干扰物质
【解析】
解:【讨论与交流】(1)加入的盐酸是少量的,碳酸钠中的氢氧化钠会先与盐酸反应,稀盐酸被耗尽,碳酸钠没有与稀盐酸反应,无法鉴别碳酸钠的有无,所以实验一不能得出正确结论;(2)碳酸根离子和酸反应会生成二氧化碳气体,所以实验二中向样品溶液滴加足量稀硝酸后不能得出正确结论,理由是:碳酸钠与稀硝酸反应,氯化钠与稀硝酸不反应,加入稀硝酸有气泡产生只能验证碳酸钠存在,无法判断氯化钠是否存在;(3)硝酸会与碳酸钠、氢氧化钠反应,所以加入稀硝酸并且至过量的目的是:除去氢氧化钠和碳酸钠,并验证碳酸钠是否存在;【归纳与总结】根据实验结论领悟到:在选加试剂检验物质成分时;既要考虑除尽原有的干扰物质,又要防止引入新的干扰物质。

 名校课堂系列答案
名校课堂系列答案【题目】用下图装置探究可燃物燃烧的条件。
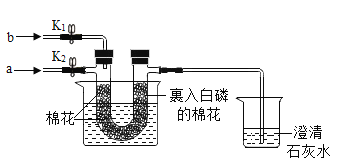
资料:棉花的着火点为210℃。
[步骤1]将U型管放入盛有冷水的烧杯中,打开K2,关闭K1,从a口通入氧气,两端均无明显现象。
[步骤2]关闭K2,打开K1,从b口通入二氧化碳,看到澄清石灰水变浑浊,然后将U型管放入盛有80℃热水的烧杯中,两端均无明显现象。
[步骤3]打开K2,关闭K1,从a口通入氧气,右端白磷先燃烧,一会儿棉花开始燃烧,此时左端棉花没有燃烧。
(1)步骤2中,通入二氧化碳的目的是________。
(2)请解释步骤3中,右端棉花燃烧的原因是_______。
(3)依据上述实验,完成下表:
该实验可以证明的燃烧条件 | 对应现象 |
温度达到着火点 | ____________ |
_____________ | 步骤2中的白磷不燃烧,步骤3中的白磷燃烧 |