题目内容
某校化学兴趣小组为测定某硝酸铵样品的纯度,将10g样品溶于30g水后,再加入13.7g氢氧化钠浓溶液共热,两者恰好完全反应(硝酸铵中的杂质不与氢氧化钠反应,也不溶于水),硝酸铵与氢氧化钠的反应方程式为:NH4NO3+NaOH NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:
NaNO3+H2O+NH3↑).把产生的所有NH3用足量的硫酸溶液吸收,同时测量2分钟内硫酸溶液增加的质量,结果如下表所示:
| 时间/s | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
(1)请在下面的坐标纸上,以反应时间为横坐标,以产生的NH3质量为纵坐标,画出能够表明产生气体的质量随时间变化的关系曲线;

(2)表中m约为______;
(3)硝酸铵样品的纯度为______;
(4)试计算反应后所得硝酸钠溶液的溶质质量分数(不考虑反应过程中水损失的质量).
解:(1)根据测定数据表中的时间与质量数据确定一些点,然后把各点利用平滑曲线图连接;绘制曲线时要做到:曲线平滑、趋势正确、给出平台;
故答案为:
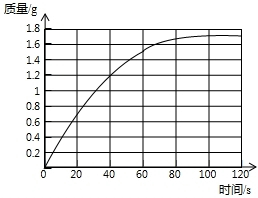
(2)根据所绘制的曲线,可估计反应进行至30s时,增加的质量约为1.0g;
故答案为:1.0g;
(3)放出1.7gNH3消耗硝酸铵的质量为m
NH4NO3+NaOH NaNO3+H2O+NH3↑
NaNO3+H2O+NH3↑
80 17
m 1.7g
 m=8g
m=8g
硝酸铵样品的纯度=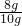 ×100%=80%
×100%=80%
故答案为:80%;
(4)设纯净硝酸钠的质量为x
NH4NO3+NaOH═NaNO3+H2O+NH3↑
85 17
x 1.7g
 x=8.5g
x=8.5g
反应后所得硝酸钠溶液的溶质质量分数= X100%=17%
X100%=17%
答:反应后所得硝酸钠溶液的溶质质量分数为17%.
分析:(1)利用数据表中测得的时间与增加的质量,找出对应的点并用平滑曲线连接;
(2)利用所绘制的曲线,查出时间为30s时所增加的质量;
(3)根据反应的化学方程式,由生成氨气的质量计算出样品中硝酸铵的质量,利用硝酸铵样品的纯度=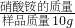 ×100%计算样品纯度;
×100%计算样品纯度;
(4)根据反应的化学方程式,由生成氨气的质量计算反应生成硝酸钠的质量,利用所得硝酸钠溶液的溶质质量分数= ×100%,反应后所得溶液质量可利用质量守恒定律进行计算而求得.
×100%,反应后所得溶液质量可利用质量守恒定律进行计算而求得.
点评:根据质量守恒定律,反应后所得硝酸钠溶液的质量=样品中硝酸铵的质量+溶解所加水的质量+氢氧化钠浓溶液的质量-反应放出氨气的质量.
故答案为:

(2)根据所绘制的曲线,可估计反应进行至30s时,增加的质量约为1.0g;
故答案为:1.0g;
(3)放出1.7gNH3消耗硝酸铵的质量为m
NH4NO3+NaOH
 NaNO3+H2O+NH3↑
NaNO3+H2O+NH3↑80 17
m 1.7g
 m=8g
m=8g硝酸铵样品的纯度=
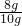 ×100%=80%
×100%=80%故答案为:80%;
(4)设纯净硝酸钠的质量为x
NH4NO3+NaOH═NaNO3+H2O+NH3↑
85 17
x 1.7g
 x=8.5g
x=8.5g反应后所得硝酸钠溶液的溶质质量分数=
 X100%=17%
X100%=17%答:反应后所得硝酸钠溶液的溶质质量分数为17%.
分析:(1)利用数据表中测得的时间与增加的质量,找出对应的点并用平滑曲线连接;
(2)利用所绘制的曲线,查出时间为30s时所增加的质量;
(3)根据反应的化学方程式,由生成氨气的质量计算出样品中硝酸铵的质量,利用硝酸铵样品的纯度=
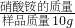 ×100%计算样品纯度;
×100%计算样品纯度;(4)根据反应的化学方程式,由生成氨气的质量计算反应生成硝酸钠的质量,利用所得硝酸钠溶液的溶质质量分数=
 ×100%,反应后所得溶液质量可利用质量守恒定律进行计算而求得.
×100%,反应后所得溶液质量可利用质量守恒定律进行计算而求得.点评:根据质量守恒定律,反应后所得硝酸钠溶液的质量=样品中硝酸铵的质量+溶解所加水的质量+氢氧化钠浓溶液的质量-反应放出氨气的质量.

练习册系列答案
相关题目




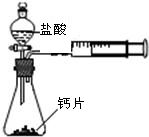
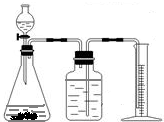
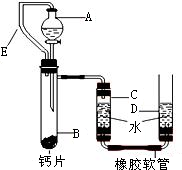
 +H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:
+H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:
