题目内容
【题目】根据下列实验装置图,回答问题:

![]()
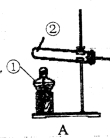
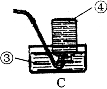
(1)写出仪器名称① ④
(2)实验室若用加热高锰酸钾的方法制取氧气,反应的符号表达式为 选用的发生装置是 (填装置代号),检查该装置气密性的方法是 ,收集较纯净的氧气可以选用的装置是
(填装置代号),选用这种收集方法的原因是 ;
(3)实验室若用过氧化氢和二氧化锰制取氧气,反应的符号表达式可以表示为 ,该反应的反应类型属于 ,二氧化锰在反应中所起的作用是 ,选用的发生装置是 (填装置代号).
(4)某同学在收集完一瓶气体后,想证明该瓶气体是氧气的方法是 .
(5)氨气(NH3)在通常状况下是一种无色有强烈刺激性气味的气体,密度比空气小,极易溶于水,其水溶液为氨水.实验室可用加热氯化铵和熟石灰两种固体混合物的方法制取氨气.实验室制取氨气应选用的发生装置是 (填字母),用的收集装置是 (填字母)
(6)某同学设计如图实验装置探究“分子的性质实验”
图I是按课本进行的一个化学实验,大烧杯中的实验现象是 ,此实验说明分子 .但是在实验时同学们闻到了一股难闻的刺激性气味,于是小明对原实验装置进行了改进,装置如图Ⅱ,并进行如下操作:
a.向B、C、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色.
b.在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟.
![]()
【分析讨论】
(1)E试管放有酚酞溶液的目的是 .
(2)改进后观察到的实验现象 ;
(3)由此又可以得到的实验结论是: .
【答案】(1)试管,酒精灯(2)2KMnO4 △K2MnO4 +MnO2 + O2↑;A;先把导管的一端浸入水中,用手握住试管,看试管口是否产生气泡;C;能把集气瓶中空气完全排尽;
(3)2H2O2![]() H2O+O2↑ ,分解反应,催化作用,B;
H2O+O2↑ ,分解反应,催化作用,B;
(4)将带火星的小木条伸入集气瓶中,若带火星的小木条复燃,说明是氧气;
(5)A,D (6)甲烧杯中的酚酞变成红色;不断的运动;
【分析讨论】(1)对比
(2)C中的酚酞比B中的酚酞更快变成红色 ;
(3)温度越高,分子运动越剧烈
【解析】
试题分析:(2)加热高锰酸钾分解制取氧气的同时,还生成了锰酸钾和二氧化锰,故反应的化学方程式是2KMnO4 △K2MnO4 +MnO2 + O2↑;根据反应物的状态和反应条件选择发生装置,用加入高锰酸钾的方法制取氧气属固固加热型,选A装置;检查装置气密性的方法是:先把导管的一端浸入水中,用手握住试管,看试管口是否产生气泡;要制取一瓶比较纯净的氧气,结合氧气难溶于水可知,可用排水 法收集,选C装置;
(3)过氧化氢在二氧化锰的催化作用下生成水和氧气;该反应的反应物是一种,生成物是两种,属分解反应,二氧化锰是该反应的催化剂,起催化作用;
(4)检验氧气的方法是将带火星的小木条伸入集气瓶中,若带火星的小木条复燃,说明是氧气;
(5)根据反应物的状态和反应条件选择发生装置,用加热氯化铵和熟石灰两种固体混合物的方法制取氨气属固固加热型,选A装置;氨气密度比空气小,极易溶于水,故只能用向下排空气法收集,选D装置;
(6)浓氨水会挥发出氨气,由于分子在不断的运动,故甲烧杯中的酚酞变成红色;
【分析讨论】E试管放有酚酞溶液的目的是起对比的作用;该进后的装置在密闭的装置内进行,不会污染空气,另增加了热水的对比实验,观察到C中的酚酞比B中的酚酞更快变成红色,说明温度越高,分子运动越剧烈。

【题目】把一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下,下列说法中正确的是
物质 | a | b | c | D |
反应前的质量 | 6.4 | 3.2 | 4.0 | 2.8 |
反应后的质量 | 5.2 |
| 7.2 | 2.8 |
A、a和c是反应物
B、d一定是催化剂
C、![]()
D、a、b的化学计量数之比一定为![]()