��Ŀ����
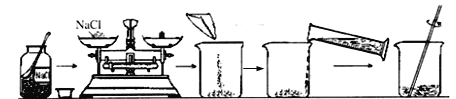
����Ŀ��ij�о���Ա����ͼ��ʾ���̽�����ȼú�����������о�����ʵ���У�SO2��O2�����������ͨ�룬ˮ��������ʼʱһ���Լ��룬��ӦҺ���ѭ����

��1�����ճ��з�����Ӧ�Ļ�ѧ����ʽ��2SO2+2H2O+O2====2H2SO4������ʱ���¶Ȳ��˹��ߵ�ԭ���� ��
��2����Ӧ���з�����Ӧ�Ļ�ѧ����ʽ�� ��Ϊȷ����ӦҺ��ѭ������Ч������Ӧ���еķ�Ӧ�������40�����ҽ��У��ڴ����������ӿ�÷�Ӧ�����˲�ȡ�Ĵ�ʩ�� ��
��3�����ŷ�ӦҺ�������ճ��У�����Һ��H2SO4�������������Լӿ죬��ԭ������� ��
��4���������ѭ����ӦҺ���������Ʊ�FeSO4��7H2O������ҽ���ϳ��������� ��ѡ����ĸ����
A����״���״� | B�����Ͳ� | C��ȣ�� | D��ƶѪ֢ |
���𰸡����� ��ֹ�¶ȹ���������ˮ�е��ܽ�ȼ�С�����������ݳ�������IJ��ʽ��� ��
�� Fe+H2SO 4 =FeSO 4+H2�� ���ý��������У�����
�� ���ɵ�Fe2+����дFeSO4�������з����ķ�Ӧ������á�
��4��D
�������������������1�����ճ��з�����Ӧ�Ļ�ѧ����ʽ��2SO2+2H2O+O2====2H2SO4������ʱ���¶Ȳ��˹��ߵ�ԭ�����¶ȹ���������ˮ�е��ܽ�ȼ�С�������ݳ�������IJ��ʽ��� ����2����Ӧ���з�����Ӧ�Ļ�ѧ����ʽ��Fe+H2SO 4 =FeSO 4+H2����Ϊȷ����ӦҺ��ѭ������Ч������Ӧ���еķ�Ӧ�������40�����ҽ��У��ڴ����������ӿ�÷�Ӧ�����˲�ȡ�Ĵ�ʩ�У��ý��������У����裻��3�����ŷ�ӦҺ�������ճ��У�����Һ��H2SO4�������������Լӿ죬��ԭ����������ɵ�Fe2+����дFeSO4�������з����ķ�Ӧ������á���4���������ѭ����ӦҺ���������Ʊ�FeSO4��7H2O������ҽ���ϳ���������ƶѪ֢����ѡ��D

 ״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�
״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�