题目内容
【题目】水是一种重要的资源。请回答下列问题:
(1)打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随_____而减小。
(2)水是一种重要的溶剂,欲配制50g溶质质量分数为10%的氯化钠溶液(水的密度是1.0g/cm3),请回答下列问题:
①称量氯化钠固体的质量为_____g;
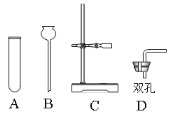
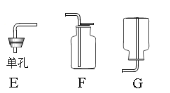
②下列仪器中必须使用的是_____(填序号)。
A.托盘天平 B.烧杯 C.玻璃棒 D.10mL量筒 E.50mL量筒
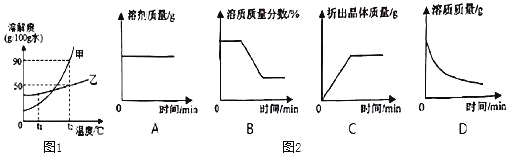
(3)甲、乙两种固体物质(不含结晶水,且不与水反应)的溶解度曲线如图1所示。
①甲、乙两种物质中溶解度受温度影响较大的是_____物质。
②若将t2℃时甲的不饱和溶液变成该温度下的饱和溶液,可采用的方法_____。(填一种即可)
③若甲物质中混有少量的乙物质,提纯甲物质可采取的方法是_____。
④t1℃时,若将25g乙固体加入50g水中,充分搅拌后,仍有9.2g乙固体未溶解,则t1℃时乙的溶解度为_____。
⑤t2℃接近饱和的甲溶液逐渐冷却至t1℃,图2中有关量随时间变化的趋势正确的是_____。(选序号)
【答案】压强的减小 5 g ABCE 甲 增加溶质 降温结晶 31.6g AB
【解析】
(1)气体的溶解度随压强的增大而增大,所以打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随压强的减小而减小;
(2)溶质质量=溶液质量×溶质质量分数,所以称量氯化钠固体的质量为50g×10%=5g;
量筒需要采用就近原则,所以配制一定质量分数溶液需要的仪器有:托盘天平,烧杯,玻璃棒,50mL量筒;
(3)①通过分析溶解度曲线可知,甲、乙两种物质中溶解度受温度影响较大的是甲物质;
②若将t2℃时甲的不饱和溶液变成该温度下的饱和溶液,可采用的方法是:增加溶质;
③甲物质的溶解度受温度变化影响较大,所以若甲物质中混有少量的乙物质,提纯甲物质可采取的方法是降温结晶;
④t1℃时,若将25g乙固体加入50g水中,充分搅拌后,仍有9.2g乙固体未溶解,所以50g水中溶解的乙固体是25g﹣9.2g=15.8g,t1℃时乙的溶解度为31.6g;
⑤t2℃接近饱和的甲溶液逐渐冷却至t1℃,溶剂的质量不变,溶质质量分数先不变,再减少,后不变,开始没有晶体析出,溶质质量应该先不变,再减少,后不变所以图2中有关量随时间变化的趋势正确的是AB。