题目内容
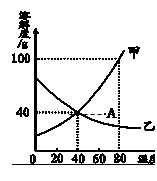
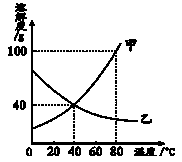
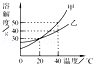
如图所示,依据甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:

(1)t1℃时,甲、乙、丙三种物质的溶解度的关系是 (用>、<或=表示 )
(2)t3℃时,甲物质饱和溶液中,溶质、溶剂、溶液的质量之比为 (填最简比).
(3)甲中含有少量的乙,若要提纯甲,可采用 的方法.
(4)t2℃时,甲、乙、丙三种物质的饱和溶液各100g,分别降温到t1℃时,所得溶液质量的关系是 (用>、<或=表示)

(1)t1℃时,甲、乙、丙三种物质的溶解度的关系是 (用>、<或=表示 )
(2)t3℃时,甲物质饱和溶液中,溶质、溶剂、溶液的质量之比为 (填最简比).
(3)甲中含有少量的乙,若要提纯甲,可采用 的方法.
(4)t2℃时,甲、乙、丙三种物质的饱和溶液各100g,分别降温到t1℃时,所得溶液质量的关系是 (用>、<或=表示)
(1)乙>甲=丙
(2)1∶2∶3
(3)降温结晶(冷却热饱和溶液)
(4)丙>乙>甲
(2)1∶2∶3
(3)降温结晶(冷却热饱和溶液)
(4)丙>乙>甲
试题分析:溶解度曲线意义:1、表示某物质在不同温度下的溶解度或溶解度随温度变化的情况,进而判断结晶的方法,①溶解度随温度的升高而增大,采用冷却热饱和溶液(即降温结晶),②溶解度随温度的升高而变化不大,采用蒸发结晶,2、两曲线的交点表示两种溶质在同一温度下具有相同的溶解度,3、可比较同温下,不同物质溶解度的大小关系,4、可直接读出某温下,物质的溶解度
(1)从曲线图可以看出:t1℃时,甲、乙、丙三种物质的溶解度的关系是:乙>甲=丙
(2)从曲线图可以看出,t3℃时,甲物质溶解度是50g,表示在100g水中达到饱和状态溶解的甲质量为50g,所以饱和溶液中,溶质、溶剂、溶液的质量之比=50:100:150=1:2:3
(3)甲中含有少量的乙,若要提纯甲,甲溶解度随温度的升高而增大,采用冷却热饱和溶液(即降温结晶)
(4)t2℃时,甲、乙两种物质的饱和溶液各100g,降温到t1℃时,结合甲、乙的曲线图,均会析出晶体,但甲溶解度随温度变化的趋势比乙溶解度随温度变化的趋势更大,所以析出的晶体量也更大,而丙的溶解度随温度升高溶解度降低,所以降温它没有晶体析出,自然溶液质量最大,所以所得溶液质量的关系是:丙>乙>甲

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目