题目内容
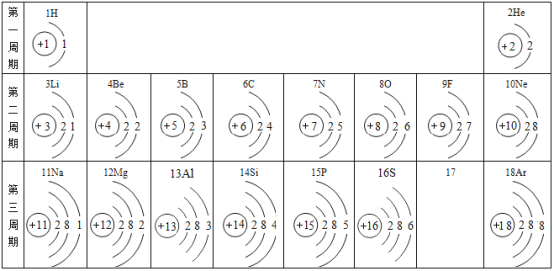
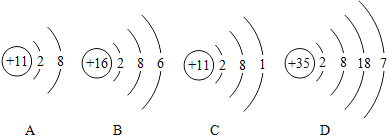
【题目】观察下列原子结构示意图和元素周期表(部分),回答有关问题。
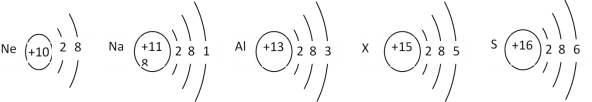
图1
(1)图1中,具有相对稳定结构的原子是_________(填元素符号)。
(2)图1中,属于金属元素的是 ________________(填元素名称)。
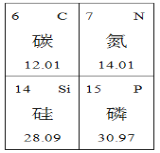
(3)含有X元素的化合物常用作化肥,X元素的原子序数是______ ,相对原子质量为 _____。
(4)硅元素的氧化物是天然水晶的主要成分。在该氧化物中,硅元素的化合价为+4价,则其化学式为 ______。
(5)在某金属单质与硫单质反应过程中,硫原子得到2个电子形成硫离子。下列说法正确的是 ________(填字母序号)。
A. 硫离子属于阴离子
B. 硫离子可表示为S2+
C. “S”既可以表示硫原子,也可以表示硫元素
D. 硫离子的核外电子数与质子数相等
(6)我国是燃煤大国,烟道气体脱硫是治理燃煤带来的环境污染的重要措施之一。
①烟道气体脱硫中的“硫”指的是___________(填字母序号)。
A. 单质 B. 元素 C. 分子 D. 离子
②烟道气体脱硫的方法之一是使煤烟中的二氧化硫(SO2)与碳酸钙和氧气反应,生成硫酸钙(CaSO4)。在将SO2转化为CaSO4的过程中,硫元素的化合价_________(填“升高”、“降低”或“不变”)。
【答案】Ne 钠、铝(少写不得分) 15 30.97(或31) SiO2 AC B 升高
【解析】
(1)元素的化学性质取决于最外层电子数,当最外层电子数为8为相对稳定结构,由图一可知,氖原子具有相对稳定结构,元素符号为Ne;
(2)由常见元素的名称可知,属于金属元素的是钠元素、铝元素;
(3)质子数为15是磷元素,原子序数是15;相对原子质量为30.97;
(4)化合物中各元素的正负化合价的代数和为零,该氧化物中,硅元素的化合价为+4价,氧元素化合价为+2,则其化学式为SiO2;
(5)硫原子最外层有6个电子,容易得到2个电子形成阴离子,故硫离子可表示为S2-;“S”既可以表示硫原子,也可以表示硫元素;硫离子的核外电子数为18,质子数为16,故硫离子的核外电子数与质子数不相等。故本题选AC;
(6)①烟道气体脱硫中的“硫”指的是硫元素;②SO2中氧元素化合价为-2,故硫元素的化合价为+4价;CaSO4中钙元素化合价为+2,氧元素化合价为-2,故硫元素的化合价+6价,故将SO2转化为CaSO4的过程中,硫元素的化合价升高。

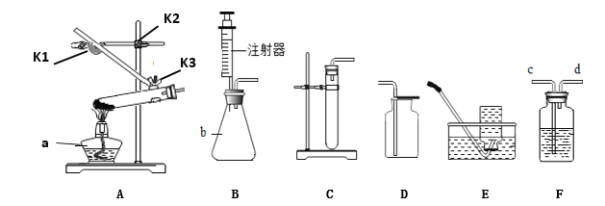
【题目】实验室常用高锰酸钾粉末制取氧气(装置A),也可以用过氧化氢溶液和催化剂二氧化锰来制取氧气(装置B)。
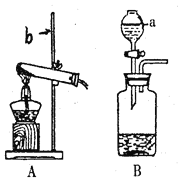
(1)标出仪器a、b的名称:a______________;b____________。
(2)写出一种实验室制取氧气的文字表达式:__________。
(3)装置A中应在试管口放_________,以防高锰酸钾粉末进入导管。
(4)从反应物状态和反应条件来比较装置A和B的差异:(补充下表)
装置A | 装置B | |
反应物状态 | ①、__________ | ②、_____________ |
反应条件 | ③、___________ | ④、_____________ |
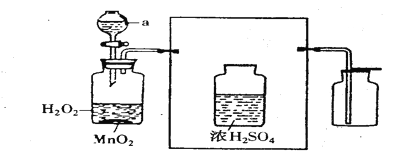
(5)用装置B制得的氧气带有少量水蒸汽,可用浓硫酸除去水蒸气,请在下列方框图中添上带橡皮塞的玻璃导管,完成除去水蒸气的实验装置图。___________