题目内容
【题目】钢铁在生产、生活中有广泛的用途:

(1)请你列举自行车链条的防锈措施_____。
(2)铁制品保存不当会生锈,铁锈的主要成分是氧化铁,用盐酸可以除去铁锈,写出盐酸除铁锈的化学方程式_________________。
(3)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什么合理的建议(答一点即可)?_____________
【答案】涂油 Fe2O3+ 6HCl =2FeCl3+ 3H2O 回收利用废旧金属 或合理开采矿物、寻找金属的代用品
【解析】
(1)自行车链条的防锈措施:涂油,防止与空气中的氧气和水蒸气接触。
(2)铁制品保存不当会生锈,铁锈的主要成分是氧化铁,用盐酸可以除去铁锈,盐酸与氧化铁反应产生氯化铁和水的化学方程式:Fe2O3+ 6HCl =2FeCl3+ 3H2O。
(3)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,还有合理的建议是:回收利用废旧金属 或合理开采矿物、寻找金属的代用品。

 阅读快车系列答案
阅读快车系列答案【题目】某校化学硏究性学习小组的成员,他们在查阅资料时,发现单质碳能够在高温时与金属氧化物反应得到金属单质。于是,他们用木炭与CuO进行了如下的探究活动请你参与他们的这次活动,并解决有关问题。
(提出问题)
木炭与氧化铜反应除生成单质铜外,还生成什么呢?
(猜想与假设)
(1)可能是CO
(2)可能是CO2
(设计方案)
为了检验CO,他们设计的方案是:把小动物放在收集的气体中,观察能否存活。后经充分研究后,认为此方案不可行,其不可行的理由是_________。
(査阅资料)
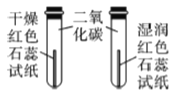
将滤纸浸泡在磷钼酸和氯化钯的黄色混合溶液中制成的试纸遇CO立即变成蓝色,而遇CO2不变色。
实验现象 | 实验结论 |
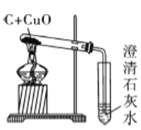
A中固体由黑色变成_________ | 有铜生成 |
B中黄色试纸没有变蓝 | 没有_______生成 |
C中__________ | 有CO2生成 |
(实验与结论)
设计的实验装置图如下:
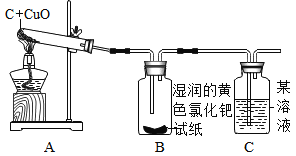
(反思与评价)
(1)对于下列三种氧化铜和炭粉的质量比,你建议选择_______(填序号)的比例,你选择的理由是_________。
A 42:3 B 40:3 C 38:3
(2)根据上述实验及学习的木炭与氧化铜、氧化铁的反应,请你归纳出单质碳的一项重要用途是_________。写出焦炭还原氧化铁的化学方程式________。