��Ŀ����
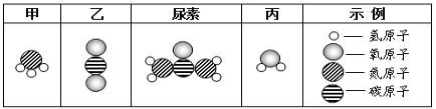
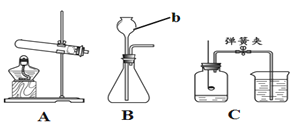
����Ŀ����7�֣���֪�������£�CO2��ˮ������������ƣ���ѧʽ Na2O2����Ӧ���� O2������CO2 �� Na2O2 ��Ӧ�Ļ�ѧ����ʽΪ 2CO2 + 2Na2O2 =2Na2CO3 +O2��ijУ��ѧ�С��Ϊ̽�� CO2��Na2O2 ��Ӧ�IJ�������ʣ����������ͼ��ʾ��ʵ��װ�á�
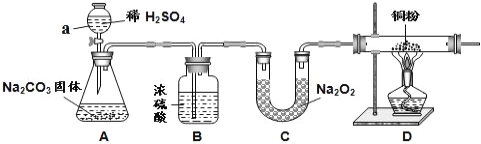
������ a �������ǣ� ��
��װ�� B �������� ��
��װ�� A �У�������Ӧ�Ļ�ѧ����ʽ ��
��װ�� D �������У����Թ۲쵽�������� ���÷�Ӧ�Ļ�ѧ����ʽΪ ��
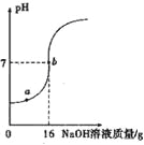
�ɷ�Ӧ��װ�� C �еĹ�����������ˮ�����Һ��Ȼ�������Һ�м��� ��ѡ����ᡱ����CaCl2 ��Һ������ʯ����Һ��֮һ��������� ������
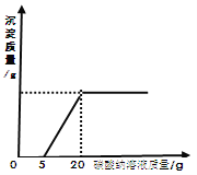
�ʷ�Ӧ��Ϻ��װ�� C �������������� 14g������� O2 ������Ϊ g��
���𰸡��� ��Һ©�� �� 8
�� ��ȥCO2�е�ˮ�������� ����CO2��
�� Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2 ��
�� ��ɫ��ĩ��� 2Cu + O2 �� 2CuO
�� ���� / CaCl2��Һ / ʯ����Һ ��ɫ���� / ��ɫ���� / ��Һ����
��������
�����������2��Ũ���������ˮ�ԣ������������
��3��̼���������ᷴӦ���������ơ�ˮ�Ͷ�����̼��Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2 ����
��4�����������������̼��Ӧ���ɵ�������ͭ��Ӧ����������ͭ���������Ǻ�ɫ�ķ�ĩ��ɺ�ɫ��
2Cu + O2 �� 2CuO��
��5�����������������̼��Ӧ���ɵ���������̼���ƣ���ôC �еĹ���������̼���ƹ��壬����������ɶ�����̼���壬���Ȼ��ƻ�����̼��Ƴ���������̼������Һ�ʼ��ԣ�������ɫʯ����Һʯ�������ɫ��
��6��װ�� C�з�����Ӧ�Ļ�ѧ����ʽΪ��2CO2 + 2Na2O2 =2Na2CO3 +O2��װ�� C �������������� 14g�����ò���������ô��������������Ϊ8g��