题目内容
【题目】实验室用下列装置来制取气体:
(1)写出有标号仪器的名称:a。
(2)利用注射器可以检查装置B的气密性。如右图所示,在锥形瓶内装适量的水,使长颈漏斗末端浸没在液面以下,将活塞缓慢往外拉, 若观察到 , 则装置不漏气。
(3)实验室制取并收集二氧化碳气体和制取并收集氧气,可选用的同一套装置组合是 , 用该装置组合制取氧气涉及的化学反应方程式是 , 实验室制CO2 , 若用C装置(多孔隔板用来放块状固体)作为制取的发生装置,其优点是(答出一点即可)。
(4)如下图所示,A管中盛有干燥的炭粉,C管中盛有干燥的氧化铜粉末,B、D两个U型管中装有碱石灰固体,用来充分吸收二氧化碳气体。现将3.0g干燥的二氧化碳气体全部缓缓通入A管进行实验,实验结束后,B管质量增加0.8g,D管质量增加3.3g,①写出实验室制取二氧化碳气体的化学反应方程式是 , ②请计算进入C管和离开C管的一氧化碳的质量各为多少 ?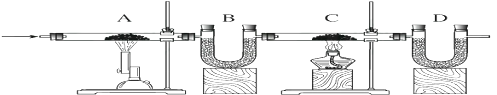
【答案】
(1)锥形瓶
(2)长颈漏斗末端有气泡冒出
(3)BD,2H2O2= 2H2O + O2↑,可以控制反应的发生和停止
(4)CaCO3 + 2HCl = CaCl2 + H2O + CO2↑,解:设与木炭反应生成的CO质量为x
m(二氧化碳) = 3.0g-0.8g = 2.2g
利用化学方程式计算得到
X = 2.8g
D管增加m(二氧化碳) = 3.3g
设还原氧化铜生成3.3g二氧化碳参加反应的CO质量是y
利用方程式计算得到:y = 2.1g
m(一氧化碳)= 2.8g-2.1g = 0.7g
答:进入C管和离开C管的一氧化碳质量分别为2.8g和0.7g
【解析】(1)根据仪器名称可知,a为锥形瓶;(2)长颈漏斗末端浸没在液面以下,将活塞缓慢往外拉时,装置内压强减少,若装置不漏气,则长颈漏斗下端会产生气泡;(3)实验室制取并收集二氧化碳气体是固液常温反应,所以要选择固液常温型装置,利用过氧化氢分解制取氧气也可选择该种装置,二氧化碳和氧气都可用向上排空气法收集,故实验室制取并收集二氧化碳气体和制取并收集氧气,可选用的同一套装置组合是BD;实验室制CO2,若用C装置(多孔隔板用来放块状固体)作为制取的发生装置,能将固体和液体分离以控制反应发生和停止,所以优点是可以控制反应的发生和停止;(4)实验室制取二氧化碳用石灰石和稀盐酸反应,生成氯化钙、水和二氧化碳;进入C管中的一氧化碳与氧化铜反应生成二氧化碳,被D吸收,所以利用方程式根据二氧化碳的质量可计算出反应的一氧化碳质量。
【考点精析】关于本题考查的二氧化碳的化学性质和书写化学方程式、文字表达式、电离方程式,需要了解化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应;注意:a、配平 b、条件 c、箭号才能得出正确答案.

 全能测控期末小状元系列答案
全能测控期末小状元系列答案【题目】对下列事实的微观解释正确的是
选项 | 事 实 | 解 释 |
A | 金刚石硬而石墨软 | 碳原子排列方式不同,金刚石分子形似足球 |
B | “干冰”升华后体积变大 | 二氧化碳分子间的间隔增大 |
C | 稀有气体是混合物 | 由不同种分子构成 |
D | 氨水和石灰水都能使紫罗兰花变蓝 | 溶液中都含有自由移动的阳离子 |
A.AB.BC.CD.D